
| A. | KCl | B. | NaF | C. | MgCl2 | D. | K2O |
分析 阳离子具有氩原子的电子层结构,说明该元素是位于第四周期的金属元素;阴离子具有氖原子的电子层结构,说明该元素是位于第二周期的非金属元素,据此解答.
解答 解:阳离子具有氩原子的电子层结构,说明该元素是位于第四周期的金属元素;阴离子具有氖原子的电子层结构,说明该元素是位于第二周期的非金属元素;
A、钾元素是位于第四周期的金属元素,氯元素是位于第三周期的非金属元素,不符合题意;
B、钠元素是位于第三周期的金属元素,氟元素是位于第二周期的非金属元素,不符合题意;
C、镁元素位于第三周期的金属元素,氯元素是位于第三周期的非金属元素,不符合题意;
D、钾元素位于第四周期的金属元素,氧元素是位于第二周期的非金属元素,符合题意;
故选:D.
点评 明确元素在周期表中的位置和元素的性质即可正确解答,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:解答题
| 常见的几种离子 | H+ Na+ Mg2+ OH- Cl- SO42- | ||
| 对应元素及原子团 在化合物中的化合价 | $\stackrel{+1}{H}$ $\stackrel{+1}{Na}$ $\stackrel{+2}{Mg}$ $\stackrel{-1}{OH}$ $\stackrel{-1}{Cl}$ $\stackrel{-2}{SO4}$ | ||
| 所能形成化合物的化学式 | 酸 | 碱 | 盐 |
| HCl H2SO4 | NaOH Mg(OH)2 | MgCl2 Na2SO4 | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 原子种类 | 质子数 | 中子数 | 核外电子数 | 相对原子质量(近似值) |
| 氢 | 1 | 1 | 1 | |
| 碳 | 6 | 6 | 6 | 12 |
| 氧 | 8 | 8 | 8 | 16 |
| 钠 | 11 | 12 | 11 | 23 |
| 铁 | 26 | 30 | 26 | 56 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 分子和原子总在不断地运动 | B. | 同种原子可能构成不同分子 | ||
| C. | 分子的质量一定大于原子的质量 | D. | 化学变化中分子可分、原子不可分 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
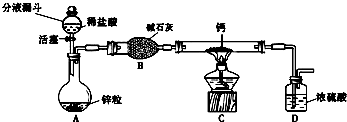
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com