
 实验室用氯酸钾与二氧化锰混合来制取氧气.现将氯酸钾与二氧化锰的混合物15g装入大试管中,加热至不再有气体生成,得到如图图象,请根据图象计算氯酸钾的质量.
实验室用氯酸钾与二氧化锰混合来制取氧气.现将氯酸钾与二氧化锰的混合物15g装入大试管中,加热至不再有气体生成,得到如图图象,请根据图象计算氯酸钾的质量. 科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 长期放置后不会分层的液体一定是溶液 | |
| B. | 配制好6%的NaCl溶液,装瓶时不小心撒漏一部分,瓶中NaCl溶液浓度仍为6% | |
| C. | KNO3饱和溶液一定比KNO3不饱和溶液溶质质量分数大 | |
| D. | 降低饱和溶液的温度,一定有晶体析出 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质 | 除杂试剂(足量) | 操作方法 |
| A | CO(CO2) | 氢氧化钠溶液 | 气体通过盛有氢氧化钠溶液的洗气瓶 |
| B | K2CO3(KCl) | 稀盐酸 | 加入稀盐酸、蒸发、结晶 |
| C | FeSO4(CuSO4) | 锌粉 | 加入锌粉并过滤 |
| D | Zn(Fe) | 稀硫酸 | 加入稀硫酸,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
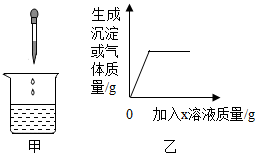 向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )
向烧杯中逐渐加入X溶液至过量(图甲),生成沉淀或气体的质量(纵坐标)与加入X溶液的质量(横坐标)关系不符合图乙的是( )| 烧杯中的物质 | X溶液 | |
| A | 稀硫酸 | 氯化钡溶液 |
| B | 氯化钠溶液 | 硝酸银溶液 |
| C | 硫酸和硫酸铜混合溶液 | 氢氧化钠溶液 |
| D | 碳酸氢钠溶液 | 稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.操作顺序 | B.生活化学 |
| ①制取O2停止加热时,先熄灭酒精灯,后撤导管 ②配制溶液需经过计算、称量、溶解等 | ①碳酸氢钠可用于治疗胃酸过多症 ②氢氧化钠可用来改良酸性土壤 |
| C.解释说明 | D.化学鉴别 |
| ①稀有气体作保护气,因为其化学性质稳定 ②一氧化碳用于冶炼金属,因为其具有还原性 | ①看颜色鉴别羊毛纤维和棉纤维 ②带火星的小木条鉴别O2和CO2 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 氧原子核内质子数为6 | B. | 硅元素位于元素周期表中第三周期 | ||
| C. | 铝离子核外有三个电子层 | D. | 铁原子的质量为55.85g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com