【答案】
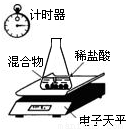
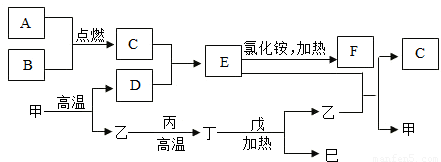
分析:(1)用氯酸钾和二氧化锰反应制取氧气需要加热反应,据此选择发生装置;又因氧气的密度大于空气的密度,并且不易溶于水,选择收集装置;然后写出化学反应式即可;大理石与稀盐酸反应制取二氧化碳,是固液在常温下反应,据此选择发生装置;根据二氧化碳密度大于空气的密度,易溶于水,选择收集装置;又因为要收集干燥的二氧化碳,所以要连接装置E;
(2)观察图示可知是固液在常温下的反应,并且收集气体的密度应小于空气的密度,然后选择即可;
(3)根据反应物是过氧化钠(Na
2O
2)与水,生成物是氧气和氢氧化钠写出化学反应式即可;因氧气不易溶于水,可用排水法收集.
(4)检验水一般用无水硫酸铜,无水硫酸铜遇水变蓝;
(5)从KCl和MnO
2混合物中回收二氧化锰,根据MnO
2不溶于水,而KCl溶于水所以可按溶解、过滤、洗涤、烘干顺序回收MnO
2;在过滤、蒸发操作中都要用到玻璃棒;
(6)若6.5g都是锌可生成氢气0.2g,而6.5g含杂质的锌也生成0.2gH
2,说明杂质也有与酸反应金属存在.再由规律:相同价态、相同质量不同种金属与足量的酸反应相对原子质量越小产生的氢气越多,做出推断.
解答:解:(1)用氯酸钾和二氧化锰反应制取氧气需要加热反应,我们可选用B作为发生装置;又因氧气的密度大于空气的密度,并且不易溶于水,可选C或D作为收集装置;反应式是:2KMnO
4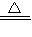
K
2MnO
4+MnO
2+O
2↑;大理石与稀盐酸反应制取二氧化碳,是固液在常温下反应,可用装置A作为发生装置;二氧化碳密度大于空气的密度,易溶于水,我们用装置D收集;又因为要收集干燥的二氧化碳,所以要在AD之间连接装置E.
具体内容如下表:
| 制取气体 | 所需药品 | 装置连接顺序 | 反应的化学方程式 |
| | | BC或BD | 2KMnO4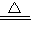 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
| | | AED | CaCO3+2HCl=CaCl2+H2O+CO2↑ |
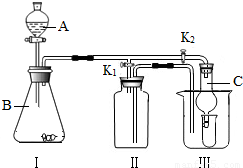
(2)根据装置I、Ⅱ的导管进出口顺序可知,装置Ⅱ只能用来收集难溶于水或密度比空气小的气体,因此利用装置I、Ⅱ可收集H
2.故选②;
(3)反应物是过氧化钠(Na
2O
2)与水,生成物是氧气和氢氧化钠,此反应的化学式是:2Na
2O
2+2H
2O═4NaOH+O
2↑;因氧气不易溶于水,可用排水法收集,改进措施是:将装置Ⅱ中装满水,打开K1,关闭K2(也就是用排水法收集氧气);
故答案为:2Na
2O
2+2H
2O═4NaOH+O
2;将装置Ⅱ中装满水,打开K1,关闭K2(也就是用排水法收集氧气).
(4)检验水一般用无水硫酸铜,无水硫酸铜遇水变蓝.故答案为:无水硫酸铜、白色粉末变成蓝色;
(5)①从KCl和MnO
2混合物中回收二氧化锰,根据MnO
2不溶于水,而KCl溶于水所以可按溶解、过滤、洗涤、烘干顺序回收
MnO
2;
②氯化钾晶体配制50g质量分数为5%的氯化钾溶液,需要氯化钾的质量为:50×5%=2.5g;
③在过滤、蒸发操作中都要用到玻璃棒,过滤实验中要用玻璃棒引流;蒸发实验中要用玻璃棒搅拌.
故答案为:①bcda;②2.5g;③C(顺序颠倒、不带单位均不给分);
(6)根据反应式计算:
设:假设6.5g金属都是锌时,可生成氢气Xg
Zn+H
2SO
4=ZnSO
4+H
2↑
65 2
6.5 X
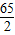
=
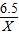
X=0.2g
可知6.5g都是锌可生成氢气0.2g,而6.5g含杂质的锌也生成0.2gH
2,说明杂质也有与酸反应金属存在,但考虑到铝、铁、镁的相对原子质量都比锌小,再由规律:相同价态、相同质量不同种金属与足量的酸反应相对原子质量越小产生的氢气越多,由此推知,杂质至少由两种金属组成,且每种组成中都含有Cu.故答案为:Cu.
点评:本题综合考查了学生的基本实验能力,涉及装置选择、连接、实验基本操作、化学计算等知识.要同学们具有综合的化学知识方可做好此题.


 K2MnO4+MnO2+O2↑;大理石与稀盐酸反应制取二氧化碳,是固液在常温下反应,可用装置A作为发生装置;二氧化碳密度大于空气的密度,易溶于水,我们用装置D收集;又因为要收集干燥的二氧化碳,所以要在AD之间连接装置E.
K2MnO4+MnO2+O2↑;大理石与稀盐酸反应制取二氧化碳,是固液在常温下反应,可用装置A作为发生装置;二氧化碳密度大于空气的密度,易溶于水,我们用装置D收集;又因为要收集干燥的二氧化碳,所以要在AD之间连接装置E.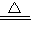 K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑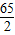 =
=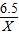


 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案