
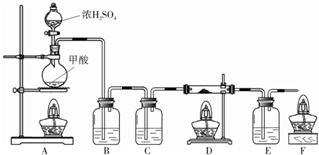
 CO↑+H2O.
CO↑+H2O. Cu+CO2 △m
Cu+CO2 △m
 ×100%=80%
×100%=80%

科目:初中化学 来源: 题型:
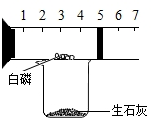 某同学用如图所示装置粗略测定空气中氧气的体积分数.图中烧杯上方玻璃管(预先固定好)中部有一左右滑动的活塞,活塞的左端内有空气,右端管口跟空气相通,实验开始前活塞处在5厘米处.实验开始时,向烧杯中加入适量水(水与生石灰反应能产生大量热使白磷燃烧).则:
某同学用如图所示装置粗略测定空气中氧气的体积分数.图中烧杯上方玻璃管(预先固定好)中部有一左右滑动的活塞,活塞的左端内有空气,右端管口跟空气相通,实验开始前活塞处在5厘米处.实验开始时,向烧杯中加入适量水(水与生石灰反应能产生大量热使白磷燃烧).则:查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
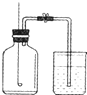 某同学用如图所示装置测定空气中氧气的体积分数.
某同学用如图所示装置测定空气中氧气的体积分数.
| ||
| ||
| 1 |
| 5 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com