
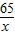 =
=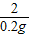 x=6.5g
x=6.5g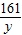 =
=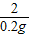 y=16.1g
y=16.1g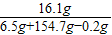 ×100%=10%
×100%=10%

 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2006?河南)图是某澄汁饮料标签上的部分内容.
(2006?河南)图是某澄汁饮料标签上的部分内容.查看答案和解析>>
科目:初中化学 来源: 题型:058
(
河南,2006)黄铜是铜和锌的合金.向一定质量的黄铜样品中加入154.7g稀硫酸,恰好完全反应,产生0.2g氢气.(1)
计算反应后所得溶液中溶质的质量分数;(2)
要计算反应后溶液中溶质的质量分数,需先求出某些物质的质量.除此之外,你还能计算出________的质量和________的质量分数(不需要具体计算).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com