


 发散思维新课堂系列答案
发散思维新课堂系列答案科目:初中化学 来源: 题型:
| A、四氯乙烷中含有8个原子 |
| B、因微溶于水,不会对富春江造成水体污染 |
| C、四氯乙烷是有机高分子化合物 |
| D、四氯乙烷中碳、氢、氯元素原子个数比为1:1:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
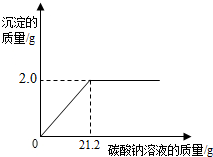 现有一包只含有氯化钙杂质的粗盐样品.某校化学小组的同学为测定该粗盐样品中氯化钙的质量分数,称取该粗盐样品10g,充分溶解于100mL水中(水的密度是1g/cm3),再滴加适量的碳酸钠溶液,产生沉淀的质量与加入碳酸钠溶液的质量关系如下图所示.试计算:
现有一包只含有氯化钙杂质的粗盐样品.某校化学小组的同学为测定该粗盐样品中氯化钙的质量分数,称取该粗盐样品10g,充分溶解于100mL水中(水的密度是1g/cm3),再滴加适量的碳酸钠溶液,产生沉淀的质量与加入碳酸钠溶液的质量关系如下图所示.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:
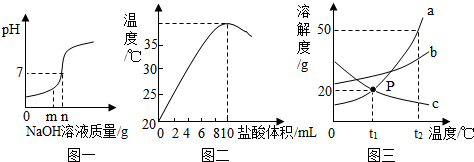
查看答案和解析>>
科目:初中化学 来源: 题型:
 如图中的甲、乙、丙表示初中化学常见的物质,且甲、乙、丙为不同类别的化合物,乙属于氧化物.胃液中含有适量的甲,可帮助消化,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物,生成物略去.
如图中的甲、乙、丙表示初中化学常见的物质,且甲、乙、丙为不同类别的化合物,乙属于氧化物.胃液中含有适量的甲,可帮助消化,图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物,生成物略去.查看答案和解析>>
科目:初中化学 来源: 题型:
 水和溶液在生活中起着十分重要的作用.
水和溶液在生活中起着十分重要的作用.| 温度/℃ | 20 | 30 | 50 | 60 | 80 | |
| 溶解度/g | K2CO3[来源:学.科.网] | 110 | 114 | 121 | 126 | 139 |
| KNO3 | 31.6 | 45.8 | 85.5 | 110 | 169 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com