
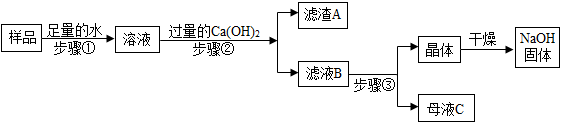
分析 (1)根据部分变质的氢氧化钠固体中含有生成的杂质碳酸钠,即部分变质的氢氧化钠固体中含有氢氧化钠、碳酸钠,步骤②是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,进行分析解答.
(2)由于氢氧化钙溶液是过量的,过滤后,滤液B为氢氧化钠和氢氧化钙的混合溶液,进行分析解答.
解答 解:(1)部分变质的氢氧化钠固体中含有生成的杂质碳酸钠,即部分变质的氢氧化钠固体中含有氢氧化钠、碳酸钠,步骤②是碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;加入过量Ca(OH)2的目的是除去溶液中碳酸钠.
(2)由于氢氧化钙溶液是过量的,过滤后,滤液B为氢氧化钠和氢氧化钙的混合溶液,滤液B中的溶质是氢氧化钠和氢氧化钙,其化学式分别是NaOH、Ca(OH)2.
氢氧化钠的溶解度随着温度的降低而减小,氢氧化钙的溶解度随着温度的降低而增大,步骤③所包含的具体操作是加热浓缩、降温结晶、过滤.
故答案为:(1)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;除去溶液中碳酸钠;
(2)NaOH;Ca(OH)2;降温结晶.
点评 本题有一定难度,熟练掌握碱的化学性质、盐的化学性质、物质结晶的方法等水蒸气解答本题的关键.


 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:初中化学 来源: 题型:解答题
 为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:
为测定某含杂质铜的锌样品中锌的质量分数,取样品20克装入一容器,再取稀硫酸200克,平均分成4份并分4次加入容器中,测定生成气体的总质量,结果如下表:| 稀盐酸的质量 | 第一次50g | 第二次50g | 第三次50g | 第四次50g |
| 生成气体总质量 | 0.2g | m | 0.6g | 0.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cr2O3 | B. | K2Cr2O7 | C. | CrO | D. | Cr |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 电解水时水中加入硫酸是为增加导电性 | |
| B. | 地球上淡水资源非常丰富 | |
| C. | 过滤能够除去水中所有杂质 | |
| D. | 水由氢气和氧气组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 凡是有发光、放热现象产生的变化一定是化学变化 | |
| B. | 物质在发生化学变化时,不一定发生物理变化 | |
| C. | 化学变化中一定伴随着放热、发光等现象 | |
| D. | 物质发生物理变化时,不一定发生化学变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com