
【题目】在一密闭容器中,有X、O2、CO2、H2O四种物质,在一定条件下发生某种反应,反应一段时间后,测得反应前后各物质的质量如下表。下列说法正确的是( )
物质 | X | O2 | CO2 | H2O |
反应前的质量/g | 19 | 34 | 6 | 2 |
反应后的质量/g | 11 | 待测 | 28 | 20 |
A.表中的待测值为32
B.X 中可能含有氧元素
C.该反应是置换反应
D.该反应中CO2和H2O的化学计量数之比为1:2
【答案】D
【解析】
根据质量守恒定律,由物质质量的增减量可确定反应物和生成物的质量,从而得出x的值,再根据物质的化学式和物质的质量可确定物质的元素组成。
A、通过质量守恒定律可知:待测值=19+34+6+2-11-28-20=2,故A错误;
B、22g二氧化碳中含有氧元素的质量为22g×![]() =16g;18g水中含氧元素的质量为18g×
=16g;18g水中含氧元素的质量为18g×![]() =16g;生成物中氧元素的质量为16g+16g=32g,与参加反应的氧气的质量正好相等,说明X中只含有碳、氢两种元素,故B错误;
=16g;生成物中氧元素的质量为16g+16g=32g,与参加反应的氧气的质量正好相等,说明X中只含有碳、氢两种元素,故B错误;
C、根据反应前后质量的变化可以判断二氧化碳和水为生成物,而X和氧气为反应物,一定不是置换反应,因为生成物二氧化碳和水都是化合物,故C错误;
D、反应中生成二氧化碳的质量为:28g-6g=22g,生成水的质量为20g-2g=18g,反应中CO2和H2O的化学计量数之比为:![]() :
:![]() =1:2,故D正确。
=1:2,故D正确。
故选:D。


科目:初中化学 来源: 题型:
【题目】燃煤产生的烟气中含有NO2、CO、SO2等物质,会严重影响大气环境,通过以下方法处理烟气,有利于实现可持续发展。
(1)利用催化剂将尾气中的一氧化碳、二氧化氮转化为两种空气中的无毒成分,反应的微观示意图如下:
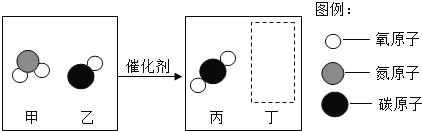
①生成物丁的微观示意图为__________。
②参加反应的甲和乙的质量比为__________。
(2)烟气中的SO2经过下列转化可以变废为宝。
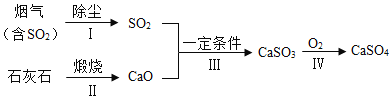
①上述物质中属于氧化物的是___________。
②过程III中发生反应的化学方程式为__________。
③上述处理过程中,化合价发生改变的元素是__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室制取气体常常用到下列装置,根据给出的装置回答下列问题:
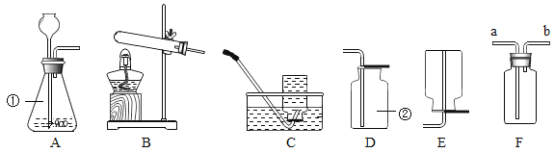
(1)写出标号仪器的名称:①____________;②____________。
(2)若选择装置A来制备氧气,请写出该反应的化学方程式____________。
(3)实验室制取二氧化碳气体,A-E中可选用的装置组合是___________(填字母),该反应的化学方程式是__________________,检验该气体是否收集满的方法___________。
(4)若选择F装置来收集二氧化碳气体,气体应从导管___________进入(选填“a”或“b”),若想收集一瓶纯净又干燥的二氧化碳,可使产生的气体连续两次通过装满液体的F装置,其中所盛的药品依次是饱和的碳酸氢钠溶液、___________(填序号)。
A 氢氧化钠固体 B 浓硫酸 C 氢氧化钠溶液
(5)小王同学用浓盐酸与大理石反应,向收集到的二氧化碳集气瓶中滴入紫色石蕊试液,观察到石蕊试液变红,对这一现象的解释不合理是__________(填序号)。
a 产生的二氧化碳直接使石蕊变红
b 产生的二氧化碳与水反应生成碳酸,使石蕊试液变红
c 挥发出的氯化氢溶于水,使石蕊试液变红
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列四个图像能正确反映其对应实验操作的是
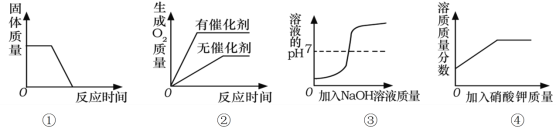
A.①高温煅烧一定质量的石灰石
B.②用等质量、等浓度的双氧水分别制取氧气
C.③向一定体积的稀盐酸中逐滴加入过量的氢氧化钠溶液
D.④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学兴趣小组参观制碱厂后,获得以下信息并对相关问题进行研究。(查阅资料)
①生产原料粗盐中含有少量可溶性杂质(MgSO4和CaC12)及不溶性杂质,生产过程中需先将粗盐精制。
②生产原理: ![]() 分离得晶体A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
分离得晶体A,并使其充分受热,可分解制得纯碱及两种常见的氧化物。
③氯化铵分解的化学方程式是: ![]()
④部分生产流程如图所示:
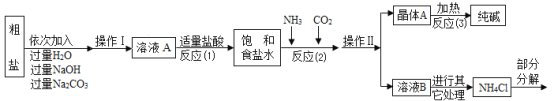
(问题讨论)
(1)①写出加入NaOH溶液所发生反应的化学方程式_______;
②操作I的名称是_________;
③反应(1)中加入适量盐酸的目的是_________;
(2)上述生产流程中可循环使用的物质是_______(填字母)。
A NH3
B NaOH
C HCl
D CO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小聪同学预配制9%的氯化钠溶液50g,整个操作过程如图所示,回答下列问题:
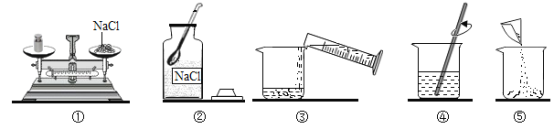
(1)配制溶液的正确操作顺序为_______(填序号,下同),其中操作错误的是_____;
(2)小聪同学配制溶液时操作不当,导致所配溶液的溶质质量分数小于9%,请分析可能的原因有哪些?(答一点)______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
说起二氧化硫(SO2),你可能首先想到它是空气质量播报中提及的大气污染物。其实你真的了解SO2吗?难道它只是有害物质吗?
SO2与食品工业
SO2作为防腐剂、漂白剂和抗氧化剂广泛用于食品行业。葡萄酒酿制中适量添加SO2,可防止葡萄酒在陈酿和贮藏过程中被氧化,抑制葡萄汁中微生物的活动。食糖加工过程中可使用SO2进行脱色。按照我国《食品添加剂使用标准(GB2760—2014)》,合理使用SO2不会对人体健康造成危害。
标准中部分食品SO2的最大残留量
食品 | 蜜饯 | 葡萄酒 | 食糖 | 水果干 | 巧克力 | 果蔬汁 |
最大残留量 | 0.35g/kg | 0.25g/L | 0.1g/kg | 0.1g/kg | 0.1g/kg | 0.05g/kg |
SO2与硫酸工业
硫酸是重要的化工原料,工业制硫酸的关键步骤是SO2的获取和转化。工业利用硫制硫酸的主要过程示意如下:
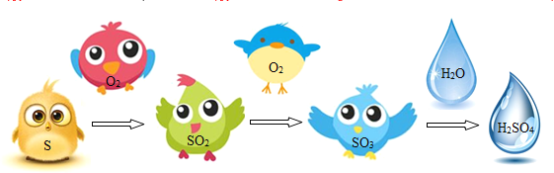
硫酸工业的尾气中含有少量SO2,若直接排放会污染空气,并导致硫酸型酸雨。工业上可先用氨水吸收,再用硫酸处理,将重新生成的SO2循环利用。
SO2与化石燃料
化石燃料中的煤通常含有硫元素,直接燃烧会产生SO2。为了减少煤燃烧产生的SO2污染空气,可以采取“提高燃煤质量,改进燃烧技术”的措施,例如,对燃煤进行脱硫、固硫处理;还可以采取“优化能源结构、减少燃煤使用”的措施,例如,北京大力推广的“煤改气、煤改电”工程,有效改善了空气质量。
现在,你对SO2一定有了新的认识,在今后的化学学习中你对SO2还会有更全面的认识!
依据文章内容回答下列问题。
(1)按照国家标准,食糖中的SO2最大残留量为____________ g/kg。
(2)葡萄酒酿制过程中SO2的作用是_________。
(3)用硫制硫酸的主要过程中,涉及到的含硫物质有S、_________和H2SO4。
(4)硫酸工业生产中,用SO3与水反应生产硫酸,发生反应的化学方程式为:_________;尾气中含有SO2气体污染空气,工业上可用___________处理尾气。
(5)下列措施能减少SO2排放的是__________(填序号)。
A 将煤块粉碎
B 对燃煤进行脱硫
C 推广煤改气、煤改电
D 循环利用工业尾气中的SO2
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是初中化学中的一些常见实验。请回答:
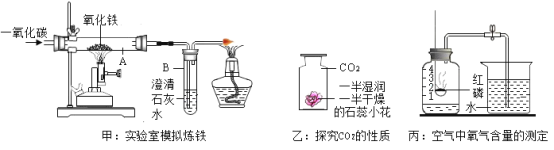
(1)甲实验进行一段时间后,在装置A和B中观察到的实验现象是________,右端导气管口酒精灯的作用是________。
(2)乙实验中,将紫色石蕊浸泡过的小花一半烘干放入盛有CO2的集气瓶中,观察到的现象是_________。
(3)下列关于丙实验的说法正确的是_______(填字母)。
A燃烧匙中的红磷越多,水位上升越高
B燃烧匙中的红磷可以换成木炭
C选用红磷是因为反应可以消耗氧气,且生成固态的P2O5
D本实验可以证明空气中含有N2、O2、CO2和稀有气体
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了保护空气,防止污染空气,某燃煤电厂采用富氧燃烧技术。
(1)分离液化空气可获得氮气和____________________两种主要气体;
(2)采用该技术有利于对CO2捕捉、封存和利用,减少碳排放,获得的CO2可用于制于冰,干冰的用途之一是_______________________;捕捉CO2可用NaOH溶液,请写出二者发生反应的化学方程式_______________________;
(3)采用此工艺,还可以使煤燃烧产生的氮氧化物和______________气体的排放总量大大下降,从而有效地防止了酸雨的形成。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com