
【题目】某硫酸溶液的酸性太强,现要调节硫酸溶液的pH,使其变大,但不能高于7,下列方法中能确保达到这一目标的最好方法是 ( )
A. 蒸发溶剂 B. 加入硝酸钡 C. 加入氢氧化钠 D. 用水稀释
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案科目:初中化学 来源: 题型:
【题目】科学家研制出以锶原子为钟摆的“晶格钟”成为世界上最精准的钟.锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( ) 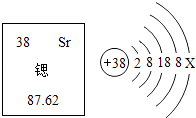
A.Sr为金属元素
B.乙图中X=2
C.锶原子的质量为87.62g
D.锶原子的质子数是38
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列有关氢氧化钠的叙述中错误的是 ( )
A. 露置在空气中易变质 B. 能使紫色石蕊试液变蓝色
C. 溶于水时放热 D. 能作为治疗胃酸过多的药物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
【假设】H2O2生成O2的快慢与催化剂种类有关.
【实验方案】常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和红砖粉,测量各生成一瓶(相同体积)O2所需的时间.
【进行实验】如图是他们进行实验的装置图,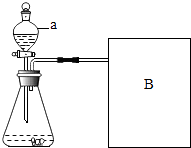
(1)气体发生装置中仪器名称:a , 此实验中B处宜采用的气体收集方法是 .
(2)【实验记录】
实验编号 | 1 | 2 |
反应物 | 5% H2O2 | 5% H2O2 |
催化剂 | 1g红砖粉 | 1g MnO2 |
时间 | 166秒 | 46秒 |
【结论】该探究过程得出的结论是
(3)、【反思】H2O2在常温下分解缓慢,加入MnO2或红砖粉后反应明显加快,若要证明MnO2和红砖粉是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的是否改变?
(4)H2O2生成O2的快慢与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响H2O2生成O2的快慢的因素以及相关假设和实验方案)
假设: .
实验方案:
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是元素周期表的一部分,据此回答下列问题. 
(1)图1中13号元素的名称是
(2)图2是元素锶(Sr)的原子结构示意图,则x= , 锶元素的氯化物的化学式为 . 通过图1分析可知,锶元素位于元素周期表第周期.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(08年苏州)现用质量分数为98%的浓硫酸(密度是1.84g·cm-3)配制560g质量分数为14%的稀硫酸时,下列有关叙述正确的是 ( )
A. 配制稀硫酸时,用到的玻璃仪器只需量筒和烧杯
B. 配制稀硫酸时,一定不能用天平称量所需浓硫酸的质量
C. 将480 mL水倾倒入盛有80 mL98%浓硫酸的500 mL量筒中
D. 将80g 98%的浓硫酸沿1000mL烧杯内壁缓缓倒入480 mL水中,并不断搅拌
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以下是某小组用过氧化氢溶液和二氧化锰反应探究影响反应速率部分因素的相关实验数据.
实验序号 | 过氧化氢溶液浓度、% | 过氧化氢溶液体积/ml | 温度/C | 二氧化锰的用量/g | 收集氧气的体积/ml | 反应所需的时间/s |
① | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
② | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
③ | 30 | 5 | 35 | / | 2 | 49.21 |
④ | 30 | 5 | 55 | / | 2 | 10.76 |
(1)请写出用过氧化氢和二氧化锰混合制取氧气的化学方程式 .
(2)通过实验①和②对比可知,化学反应速率与有关;从实验③和④对比可知,化学反应速率与温度的关系是 .
(3)【拓展延伸】上述实验中,该小组采用了控制变量的研究方法.用此方法探究“催化剂对用过氧化氢溶液制取氧气的反应速率的影响”,需要控制不变的因素有(答出两点即可)、等.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com