
【题目】下列图象与对应实验不符合的是
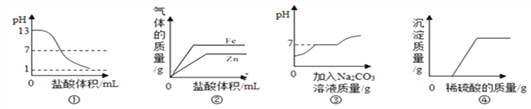
A. 图①表示向pH=13的氢氧化钠溶液中逐滴加入pH=1的盐酸
B. 图②表示向等质量的锌、铁粉末中分别滴加足量相同浓度的稀盐酸
C. 图③表示向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液
D. 图④表示向氢氧化钠与氯化钡的混合溶液中逐滴加入稀硫酸
【答案】BD
【解析】
A、pH=13的氢氧化钠溶液中逐滴加入pH=1的盐酸发生中和反应,生成中性物质,碱性不断减弱至恰好反应时pH=7,再滴加盐酸酸性会不断增强,但不可能达到pH=1,正确;B、等质量的锌、铁与足量的稀盐酸反应,由于横坐标是加入盐酸的体积,斜率应该相同,因为是在金属中滴加相同质量的酸,产生氢气的斜率只和滴加盐酸的速率有关,与图象不一致,错误;C、向盐酸和氯化钙的混合溶液中不断滴加碳酸钠溶液时,碳酸钠先和稀盐酸反应,溶液酸性减弱,pH升高,恰好完全反应时溶液pH=7, 碳酸钠和氯化钙生成碳酸钙和氯化钠的过程中pH不变,继续加入碳酸钠溶液时,溶液显碱性,pH大于7,正确;D、向氢氧化钠与氯化钡的混合溶液中逐滴加入稀硫酸,一开始就会有硫酸钡沉淀生成,而图象反映的是一开始滴加时无沉淀生成,错误。故选BD。


 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案科目:初中化学 来源: 题型:
【题目】一些骗子常用黄铜冒充黄金骗取钱财,某同学通过查阅资料得知黄铜是锌和铜的合金,他取一定量的某黄铜样品放入烧杯中,再向其中分4次加入等质量的同一稀硫酸,每次均充分反应。实验过程中有关物质的用量及质量测定记录如下表:
实验次数 | 1 | 2 | 3 | 4 |
稀硫酸的用量/g | 20 | 20 | 20 | 20 |
剩余固体的质量 | 10 | 8.7 | 7.4 | 7.2 |
分析表中数据,完成下列问题:
(1)所取黄铜样品的质量为___________ g;
(2)第4次实验结束后溶液的pH __________7(填“>”、“=”或“<”);
(3)所用稀硫酸中溶质的质量分数为________________?(要求有解答过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是实验室常用的装置,请根据要求回答问题。
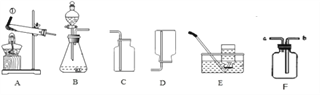
(1)仪器①的名称:___________________;
(2)实验室用氯酸钾和二氧化锰制取 O2 的化学方程式为_____,选 用的气体发生和收集装置是_____(填装置序号);
(3)实验室可用氧化钙固体与浓氨水在常温下混合制取氨气(NH3),选用的气体发生装置 是_____(填装置序号);
(4)图中的 C、D、E 三种装置,均可用如图所示的 F 装置代替,若用 F 装置进行排空气 法收集 CO2,CO2 从 F 装置的___________ (填”a”或“b”,下同)导管口通入,若要得到干燥的 O2,可先在F 装置中装______________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A、B、C、D 均含有同一种元素,它们的转化关系如右图(部分物质和反应条件乙略去).
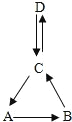
若 C 的溶液呈蓝色,D 是难溶性碱,则 B 的化学式为____________,由 D→C 的化学方程式____________________.
若C是相对分子质量为100的盐,B可用于配制农药波尔多液,则D的化学式为_______________,由 C→A 的基本反应类型为_____________________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学为了测定一瓶过氧化氢溶液中溶质的质量分数,取该溶液68.0g,加入二氧化锰2.0g,待完全反应不再有气体逸出时,称得得剩余物质的总质量为68.4g。计算:
(1)反应完全后产生氧气的质量是__________g。
(2)该过氧化氢溶液中溶质的质量分数(写出计算过程)___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纳米材料常常具有一些特殊性质,纳米铁粉在隐形材料喷涂方面有着球形铁粉无可比拟的优越性,广泛用于国防军工领域,某化学小组通过动手实验制备纳米铁粉。
(查阅资料)
(1)用硫酸亚铁、草酸(H2C2O4)两溶液发生复分解反应来制备草酸亚铁(FeC2O4)。
常温下,草酸亚铁的溶解度较小。
(2)焙烧草酸亚铁: FeC2O4 ![]() Fe+2CO2↑。
Fe+2CO2↑。
(3)纳米铁粉在空气容易被氧化生成氧化铁。
(实验步骤)

(1)草酸亚铁晶体的制备如图1
①若配制的硫酸亚铁溶液略呈黄色,可能原因是___________________;
②写出硫酸亚铁与草酸溶液反应的化学方程式_________________;
③为了分离所得固体沉淀物,需要的玻璃仪器有烧杯、玻璃棒_______;
④用冰水洗涤固体沉淀物到 pH =7为止的目的是_________________;
(2)纳米铁粉的制备如图2
将一根玻璃管在酒精喷灯上烧制成如图2所示形状,向其中加入黄色草酸亚铁晶体.当草酸亚铁粉末受热完全变黑,立即将管口部分放在火焰烧熔封闭,这样便得到了高纯度的纳米铁粉。
①分解草酸亚铁的实验中所产生的CO2对于该实验步骤所起的作用是________。
②指导老师提醒同学们应准确把握玻璃管的烧熔封闭时间.你认为烧熔过早、过晚的后果分别是______________________,___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】FeCl2溶液中混有少量的CuCl2,为了除去CuCl2,某课外小组同学取该溶液50g于烧杯中,然后等量分5次加入某物质M充分反应,所得数据如下表,请根据相关知识和数据回答下列问题:
次数 | 1 | 2 | 3 | 4 | 5 |
加入M的质量(g) | 0.28g | 0.28g | 0.28g | 0.28g | 0.28g |
溶液的总质量(g) | 49.96 g | 49.92 g | 49.88g | 49.84g | 49.84g |
(1)写出物质M的化学式______.
(2)参加反应M的总质量是________?
(3)FeCl2溶液中CuC12的质量分数是_______?
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】中和反应在工农业生产和生活中有广泛的应用。某化学实验小组的同学对酸碱中和反应进行了如下研究。
(实验过程1)
对于没有明显实验现象的中和反应,如稀盐酸与稀氢氧化钠溶液的反应,要证明它们之间确实发生了化学反应,可通过下图所示实验步骤进行操作。
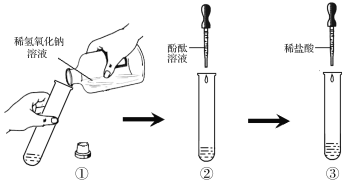
请根据上图所示实验步骤填写实验报告:
实验步骤 | 实验现象 | 实验结论 |
①向试管中加入1~2ml稀氢氧化钠溶液 | NaOH与HCl 发生了中和反应 | |
②_______________ | ______________ | |
③____________ | ______________ |
(实验过程2)
对于某些有明显现象产生的中和反应,如稀盐酸与氢氧化铝的反应,观察到有___的现象,就可以说明中和反应已经发生。该反应的化学方程式为_____。〔提 示:氢氧化铝是不溶于水的白色固体,其化学式为Al(OH)3〕
(实验反思)
(1)有同学提出也可以使用石蕊溶液代替酚酞溶液进行(实验过程1)的实验。你认为______(填“酚酞溶液”或“石蕊溶液”)更适合用于验证稀盐酸与稀氢氧化钠溶液发生中和反应,你的理由是_____。
(2)对于没有明显现象出现的酸碱中和反应,我们可以借助_____的变化,来判断是否反应或反应进行的程度。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某校化学小组在利用硫酸和氢氧化钠溶液探究酸碱中和反应时,测得烧杯中溶液 pH 的变化如图所示。下列说法正确的是( )
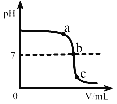
A. a 点所示溶液呈酸性
B. 向 b 点所示溶液中滴加石蕊溶液,溶液呈紫色
C. 该实验是将 NaOH 溶液逐滴滴入稀硫酸中
D. c 点所示溶液中,含有的溶质是 Na2SO4和 NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com