
| A.Al﹥Ag﹥X | B.Ag﹥X﹥Al | C.Al﹥X﹥Ag | D.X﹥Al﹥Ag |
科目:初中化学 来源:不详 题型:单选题
| A.X Y Z | B.Z Y X | C.Y Z X | D.X Z Y |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.电解水实验说明水由氢、氧两种元素组成 |
| B.用黄铜片在铜片上刻划实验说明合金一般比纯金属硬度大 |
| C.NaOH溶于水实验说明化学反应在生成新物质的同时还放出热量 |
| D.向镁、锌、铁、铜中分别加入盐酸的实验得出镁、锌、铁的金属活动性比铜强 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:填空题
| 实验 编号 | 容器I | 针筒I | 容器II | 针筒II | 红墨水 液面位置 |
| a | | 10ml 水 | NaCl | 10ml 水 | 保持 左高右低 |
| b | 二氧化碳 (充满) | 10ml 澄清石灰水 | 二氧化碳 (充满) | 10ml 浓氢氧化钠溶液 | |
| c | 1g锌 | 15ml盐酸 | 1g镁 | 15ml盐酸 | |

查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.X的化学式是H2 | B.NaAlO2属于氧化物 |
| C.此反应不属于复分解反应 | D.铝锅不宜长时间盛放碱性食品 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.甲>乙>丙>丁 | B.乙>甲>丙>丁 |
| C.丁>两>乙>甲 | D.乙>甲>丁>丙 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
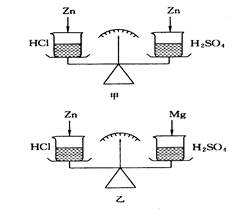
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.铁丝分别放入硝酸铜溶液和硝酸银溶液 |
| B.铁丝放入硝酸铜溶液,铜丝放入硝酸银溶液 |
| C.铜丝放入硝酸亚铁溶液,铁丝放入硝酸银溶液 |
| D.银丝分别放入硝酸铜溶液和硝酸亚铁溶液 |
查看答案和解析>>
科目:初中化学 来源:不详 题型:单选题
| A.Mg>R>Cu | B.Cu>R>Mg | C.R>Mg>Cu | D.Mg>Cu>R |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com