
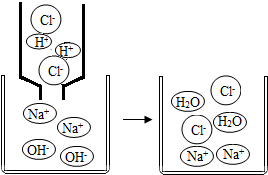
 初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-═H2O.如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式.离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)
初中化学中,我们学习了酸和碱发生中和反应的实质是H++OH-═H2O.如图,像这种用实际参加反应的离子符号来表示反应的式子叫离子方程式.离子方程式的书写一般按以下步骤:(以Na2SO4与BaCl2反应为例)分析 根据反应原理写出反应的化学方程式;
(1)离子之间不反应生成气体、沉淀、弱电解质或络合物或发生氧化还原反应、双水解反应的就能共存,据此分析解答.
(2)反应生成氯化钙、水、二氧化碳,水、二氧化碳、碳酸钙在离子反应中保留化学式;
(2)反应生成KCl和碘,氯气、碘在离子反应中保留化学式.
(3)非氧化性的强酸如稀硫酸、稀盐酸与金属镁的反应.
(4)复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,生成物中有气体或沉淀或水;反应就能发生.
解答 解:Na2SO4与BaCl2反应的化学方程式:Na2SO4+BaCl2=BaSO4↓+2NaCl;
(1)A.这几种离子之间不反应,所以能大量共存,故正确;
B、H+ 和OH- 反应生水,故错误;
C、这几种离子之间不反应,所以能大量共存,故正确;
D.H+ 和 CO32- 反应生成二氧化碳和水,故错误;
(2)石灰石和盐酸反应的离子反应为:CaCO3+2H+=Ca2++H2O+CO2↑;故填:CaCO3+2H+=Ca2++H2O+CO2↑;
(3)与离子方程式Mg+2H+=Mg2++H2↑相对应的化学方程式:Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑;故填:Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑.
(4)复分解反应实质上就是两种化合物在溶液中相互交换离子的反应,生成物中有气体或沉淀或水;反应就能发生.故填:水.
答案:Na2SO4+BaCl2=BaSO4↓+2NaCl
(1)AC;
(2)CaCO3+2H+=Ca2++H2O+CO2↑;
(3)Mg+H2SO4=MgSO4+H2↑或Mg+2HCl=MgCl2+H2↑.
(4)水.
点评 本题考查的是复分解反应的条件和复分解反应的实质,完成此题,可以依据已有的知识进行.


 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案科目:初中化学 来源: 题型:实验探究题
 我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和木炭粉为原料值得来黄铜(铜和锌的合金,外观似黄金),其生产流程如下:
我国古代将炉甘石(主要成分:ZnCO3)、赤铜矿(主要成分:Cu2O)和木炭粉为原料值得来黄铜(铜和锌的合金,外观似黄金),其生产流程如下:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
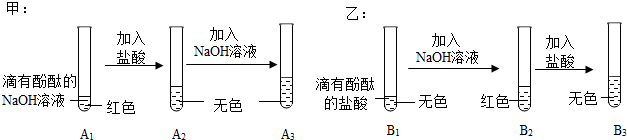
| 探究 环节 | 甲同学的探究 | 乙同学的探究 |
| 提出 问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 做出 猜想 | 实验过程中,酚酞变质了? | 猜想一:NaCl 猜想二:NaCl HCl |
实验 验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想不成立(填“成立”或“不成立”) (2)你认为在常温下A2溶液测出的pH <(填“>”、“=”或“<”)7 | 取少量B3溶液加入盛有少量铁粉的试管中,观察到有无色气泡产生,固体逐渐减少,溶液由无色变浅绿色,你认为乙同学的猜想二.(填“一”或“二”)成立 |
交流 反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是NaOH+HCl=NaCl+H2O. (2)A3溶液未变红,你认为原因是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和. (3)甲、乙同学经过实验对比探究,认为做化学实验时应注意药品用量的控制. | |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
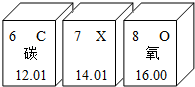 如图为元素周期表的一部分(x元素信息不全).下列说法正确的是( )
如图为元素周期表的一部分(x元素信息不全).下列说法正确的是( )| A. | 碳的化学性质活泼 | B. | X表示N2 | ||
| C. | 氧原子的质子数是8 | D. | 三种元素原子的核外电子数相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
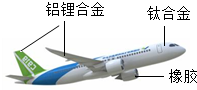 2015年11月,我国首架大型客机C919(如图)正式下线,实现了我国航空领域的新突破.回答下列问题:
2015年11月,我国首架大型客机C919(如图)正式下线,实现了我国航空领域的新突破.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁条在空气中剧烈燃烧,发出耀眼白光,生成黑色固体 | |
| B. | 铁锈在稀盐酸里浸泡一段时间后,铁锈消失,溶液变为浅绿色 | |
| C. | 向淀粉溶液中滴加碘水,溶液变为蓝色 | |
| D. | 向硫酸铜溶液中滴加氢氧化钠溶液,生成白色沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
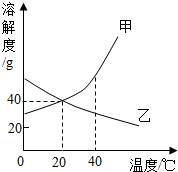 甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体物质的溶解度曲线如图所示,下列说法正确的是( )| A. | 20℃时,甲物质的溶解度是40 | |
| B. | 升温可使乙物质的饱和溶液析出固体 | |
| C. | 甲物质的溶解度大于乙物质的溶解度 | |
| D. | 40℃时,将甲、乙两物质饱和溶液分别降温到20℃,二者都变为不饱和溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com