
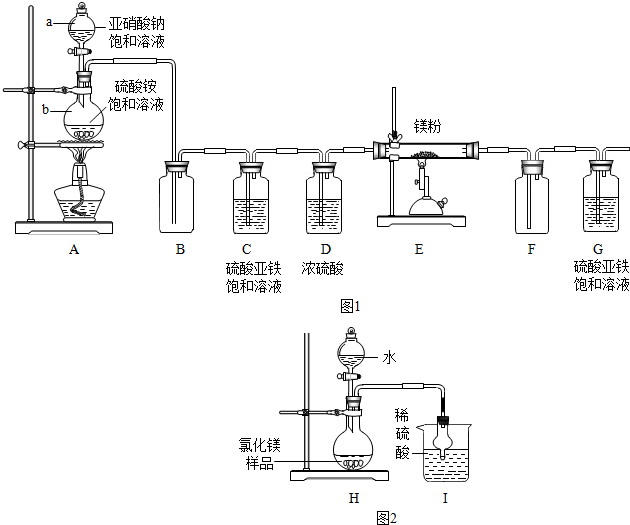
分析 (1)装置内含有氧气、反应生成的气体中可能含有氮的氧化物,装置C除去氧气(及氮氧化物)、D干燥氮气,防止对E装置反应的影响;C、D对调后无法除去水蒸气;
(2)装置E中氮气与镁反应生成二氮化三镁;
(3)根据进行实验时先进行A处加热,为了排尽空气解答;
(4)若Mg有剩余,将上述反应后的上清液去掉,加入盐酸,有气泡生成;
(5)根据球形干燥管的作用是充分反应,防倒吸解答;
根据I装置增重3.4克为氨气的质量,利用化学方程式分析解答;
根据致该样品中氮化镁含量测定结果偏低的可能原因是产生的氨气未能全部被吸收解答.
解答 解:(1)浓硫酸具有吸水性,能够吸收水蒸气(干燥氮气);G装置的作用是防止空气中的氧气进入E装置;D干燥氮气,除去水蒸气,防止对E装置反应的影响;C、D对调后无法除去水蒸气,故C、D不能对调,故填:吸收水蒸气(干燥氮气);防止空气中的氧气进入E装置;否;
(2)装置E中氮气与镁反应生成二氮化三镁,反应方程式为:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;故填:3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
(3)进行实验时先进行A加热,理由是排尽空气;故填:排尽空气;
(4)弃去上清液,加入盐酸,若观察到有气泡产生,则证明产物中含有未反应的镁,反应的方程式:Mg+2HCl═MgCl2+H2↑;
故填:Mg+2HCl═MgCl2+H2↑;
(5)①球形干燥管的作用是充分反应,防倒吸;故填:充分反应,防倒吸;
②设样品中氮化镁的质量为x
Mg3N2+6H2O═3Mg(OH)2+2NH3↑
100 34
x 3.4g
$\frac{100}{34}=\frac{x}{3.4g}$
x=10g
该样品中氮化镁的质量分数=$\frac{10g}{20g}$×100%=50%
故填:50%;
③致该样品中氮化镁含量测定结果偏低的可能原因是产生的氨气未能全部被吸收.
故填:产生的氨气未能全部被吸收.
点评 本题以氮化镁的制备为载体,考查学生对实验装置的理解、元素化合物的性质、实验方案的设计等,是对学生综合能力的考查,需要学生基本扎实的基础与分析问题、解决问题的能力.


科目:初中化学 来源: 题型:选择题
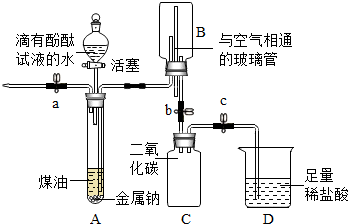 金属钠在空气中极易被氧化,常温下能与水剧烈反应生成氢氧化钠和氢气.化学兴趣小组同学在老师指导下设计了下图所示装置进行实验探究(支持装置已略去).已知:该装置气密性良好;煤油不与金属钠反应;煤油密度比水小且不溶于水.
金属钠在空气中极易被氧化,常温下能与水剧烈反应生成氢氧化钠和氢气.化学兴趣小组同学在老师指导下设计了下图所示装置进行实验探究(支持装置已略去).已知:该装置气密性良好;煤油不与金属钠反应;煤油密度比水小且不溶于水.| 步骤 | 操 作 | 现 象 |
| Ⅰ | 先打开a,再打开分液漏斗活塞.待大试管A中充满液体后,立即关闭a及分液漏斗活塞 | A中液体分层,油层在上.钠熔成银白色小球,在液体的界面处剧烈反应,产生大量气泡;下层溶液呈红色,并逐渐进入B中 |
| Ⅱ | 打开b,待B中部分溶液进入C中时关闭b,并打开a排气减压 | C中溶液仍呈红色 |
| Ⅲ | 打开止水夹c | D中溶液进入C中,产生气泡,溶液变为无色 |
| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 检查装置气密性时,先用双手紧贴试管外壁,再将导管的一端浸入水中 | |
| B. | 使用H2O2溶液和MnO2制氧气时,先将药品装入装置,然后检查装置的气密性 | |
| C. | 使用滴管时,先用手指捏紧橡胶乳头,然后把滴管伸入试剂瓶中,放开手指,吸入液体试剂 | |
| D. | 实验室制取、收集氧气时,先将导气管伸入盛满水的集气瓶,再给试管加热 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 加入的氢氧化钠溶液的质量/g | 40 | 80 | 120 | 160 |
| 生成沉淀的质量/g | 0 | 9.8 | 19.6 | 19.6 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①③⑥ | B. | ①②⑤ | C. | ③④⑥ | D. | ①②④ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 活性炭可除去水中的异味但不能降低水的硬度 | |
| B. | 使用农药、化肥对人类有利也有弊 | |
| C. | 商家用甲醛溶液浸泡海产品保鲜对顾客有益 | |
| D. | 食用加铁酱油、加碘食盐等可补充人体健康必需的化学元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com