
| 操 作 | 现 象 | 结 论 |
| | | |
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:
| 烧杯中可能出现的现象 | 结论 |
| ① | 只含C |
| ② | 含C、CuO |
| ③有黑色不溶物,有气泡逸出,溶液呈浅绿色 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 烧杯中可能出现的现象 | 结论 |
| ①有黑色不溶物,无气泡逸出,溶液呈无色 | 结论:只含 |
| ② |
结论:含C、CuO |
| ③ |
结论:含C、Fe |
| ||
| ||
| ||
| 实验步骤 | 现象 | 结论 |
| 猜想①不正确 |
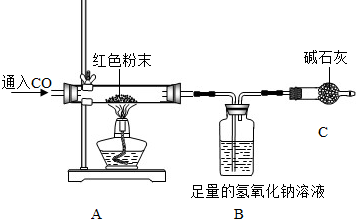
查看答案和解析>>
科目:初中化学 来源: 题型:
| 烧杯中可能出现的现象 | 结论 |
| ① ①无明显现象,固体质量不减少,且溶液仍为无色 ①无明显现象,固体质量不减少,且溶液仍为无色 . |
只含C |
| ② 有黑色不溶物,溶液由无色变为黄色 有黑色不溶物,溶液由无色变为黄色 . |
含C、Fe2O3 |
| ③有黑色不溶物,有气泡逸出,溶液呈浅绿色 | 含 C、Fe C、Fe |
查看答案和解析>>
科目:初中化学 来源:不详 题型:问答题
| 烧杯中可能出现的现象 | 结论 |
| ①______. | 只含C |
| ②______. | 含C、Fe2O3 |
| ③有黑色不溶物,有气泡逸出,溶液呈浅绿色 | 含______ |
查看答案和解析>>
科目:初中化学 来源:2011年江苏省泰州市靖江外国语学校中考化学二模试卷(解析版) 题型:解答题
| 烧杯中可能出现的现象 | 结论 |
| ①有黑色不溶物,无气泡逸出,溶液呈无色 | 结论:只含______ |
| ②______ | 结论:含C、CuO |
| ③______ | 结论:含C、Fe |
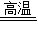 2Cu+CO2↑,4CuO
2Cu+CO2↑,4CuO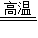 2Cu2O+O2↑
2Cu2O+O2↑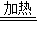 2Cu+CO2,Cu2O+2HCl=CuCl2+Cu+H2O
2Cu+CO2,Cu2O+2HCl=CuCl2+Cu+H2O| 实验步骤 | 现象 | 结论 |
| ______ | ______ | 猜想①不正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com