��2013?�»��ж�ģ��ij��ѧ���μ��˻�ѧʵ�鼼�ܿ��飮
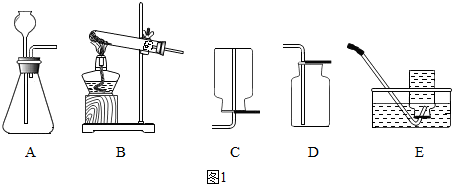
��l��С���鵽����Ŀ�ǡ�������ʵ�����Ʒ�--�ü��ȸ�����صķ�����ȡ��������
��ͼ1��a������������
ˮ��
ˮ��
��
��С����ͼ��ѡȡ��װ����
BD��BE
BD��BE
��������ţ�
�۸÷�Ӧ�Ļ�ѧ����ʽ��
��
��Bװ���е�����������
��ֹ������ط�ĩ��������
��ֹ������ط�ĩ��������
��
��2��С��鵽����Ŀ�ǡ�������̼��ʵ�����Ʒ�����ʵ��������ҩƷ����ͼ2��ʾ�ij���������
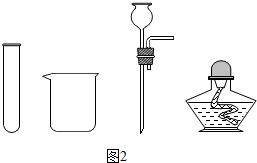
ҩƷ��ϡ���ᡢ��״ʯ��ʯ��̼���Ʒ�ĩ������ʯ��ˮ
С���һ��ѡ��������װ�÷���װ�ã��ڶ�������װ�õ�װ���м�������ҩƷ���۲쵽��Ӧ�dz����ң���Ѹ��ֹͣ���������ռ�������̼��������
�ٵ�һ��С�ⲻ��Ҫ�õ�����������
�ƾ���
�ƾ���
��
�ڵڶ���С��ѡȡ�Ĺ���ҩƷ��
̼���Ʒ�ĩ
̼���Ʒ�ĩ
��
�۵�����С�������IJ���������
��ȼ�ŵ�ľ�������ڼ���ƿ�ڣ���ľ��Ϩ�����ռ�����
��ȼ�ŵ�ľ�������ڼ���ƿ�ڣ���ľ��Ϩ�����ռ�����
��
��С�����������ȱ�ٵ�ʵ�鲽����
���װ�õ�������
���װ�õ�������
��





 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
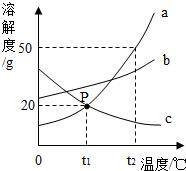 ��2013?�»��ж�ģ����ͼA��B��C���ֹ������ʵ��ܽ�����ߣ�A��C���������ܽ�����ߵĽ���ΪP���ش�����������⣺
��2013?�»��ж�ģ����ͼA��B��C���ֹ������ʵ��ܽ�����ߣ�A��C���������ܽ�����ߵĽ���ΪP���ش�����������⣺