
【题目】下图1为甲、乙两种固体物质的溶解度曲线。
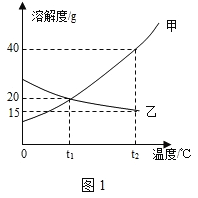
(1)溶解度随温度升高而增大的物质是________(填 “甲”或“乙”)。
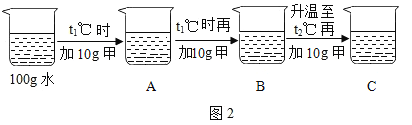
(2)某同学按图2所示进行实验,得到相应温度下的A、B、C溶液,在A、B、C三种溶液中属于饱和溶液的是________(填字母)。向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,所得溶液中溶质的质量分数为________(结果精确到0.1%)。
(3)将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,所得溶液中溶质的质量分数甲________乙(填“<”、“=”或“>”)。
(4)将t2℃时70 g 甲的饱和溶液稀释为质量分数为10%的溶液,需加水的质量为________。
【答案】甲 B 28.6% > 130g
【解析】
由溶解度曲线可知,甲物质溶解度随着温度下降而减小,乙物质溶解度随着温度下降而增大。
(1)由溶解度曲线可知,甲物质溶解度随温度升高而增大。
(2)由溶解度曲线可知,在t1℃时甲物质溶解度为20g,向100g水中加入10g甲物质形成不饱和溶液即A,再加10g甲物质形成饱和溶液即B,在t2℃时甲物质溶解度为40g,然后继续向B中加入10g甲物质,即100g水中加入30g甲,形成不饱和溶液即C,向溶液C中再加入25g甲,充分搅拌,恢复到t2℃时,只能溶解40g甲物质形成饱和溶液,所得溶液中溶质的质量分数为![]() 。
。
(3)根据溶解度曲线可知,甲物质溶解度随着温度下降而减小,乙物质溶解度随着温度下降而增大,所以将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃,甲溶液中有晶体析出,计算此时溶液中溶质质量分数利用t1℃时饱和溶液溶解度,乙溶液变为不饱和溶液,降温过程中乙溶液中溶质质量分数不变,计算此时溶质质量分数利用t2℃饱和溶液溶解度,饱和溶液溶解度越大,其溶质质量分数越大,所以所得溶液中溶质的质量分数甲>乙。
(4)t2℃时,甲物质的溶解度是40g,所以将70g乙的饱和溶液稀释为质量分数为20%的溶液,需加水的质量为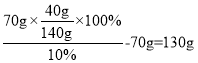 。
。


 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
(1)人体中骨骼与牙齿的重要成分是羟基磷酸钙[Ca10(PO4)6(OH)2],羟基磷酸钙由_____种元素组成。
(2)二氧化碳、铜和氯化钠三种物质中,由分子构成的是_____。
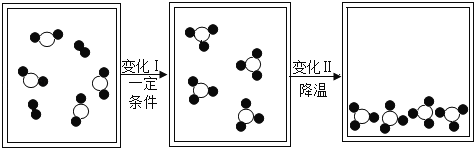
(3)某密闭容器中物质变化过程的微观示意图如图,请回答:
变化Ⅰ表示的宏观事实是_____;(填“物理变化”或“化学变化”)
变化Ⅰ中的二氧化硫、氧气、三氧化硫的分子个数比_____。
(已知:●代表氧原子,〇代表硫原子)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你参与下列探究:
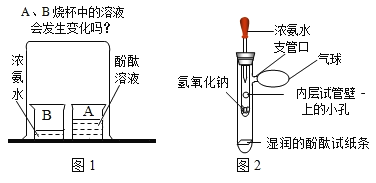
(问题情景)在课堂上老师给大家做关于分子运动的演示实验。(见图1)同学们都闻到了刺激性的氨味。
于是,课外活动小组的同学们在老师的指导下,设计了如图2的实验装置,进行同样的实验,结果不再有刺激性的氨味,并且快速出现实验现象,得到了和课本实验同样的结论。
(查阅资料)氢氧化钠溶于水放出大量的热,但不与氨水发生化学反应
(实验探究与结论)同学们用图2装置进行实验。
(1)滴入少量浓氨水后,湿润的酚酞滤纸条变成了红色,从分子的角度分析,此现象可说明的结论是______________。
(2)放氢氧化钠的目的是_________________。从而说明了分子运动与_____________有关。
(3)和课本实验比较,小明改进后的装置的优点是(写出一点)_________________。
(交流与讨论)同学们通过讨论还发现采用图2的装置还可以制取氧气。请你猜猜看他们在内层试管中装的药品是_____________,在胶头滴管中装的药品是_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于四种粒子的结构示意图的说法中正确的是( )

A. 共有四种元素
B. ①属于阳离子④属于阴离子
C. ①③的化学性质相似
D. ①④已达到相对稳定结构
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组利用下列装置进行气体的实验室制取和收集实验,请回答:
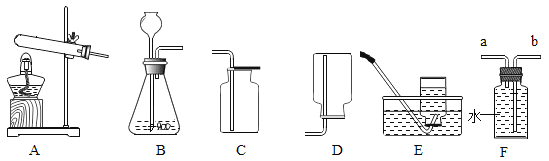
(1)若用高锰酸钾制取氧气选用的发生装置是___________(填装置序号)。你认为该装置存在的缺陷是____________。
(2)若用过氧化氢制取氧气,发生反应的化学方程式是_________,若要收集较为纯净的氧气,则选用__________(填装置序号)。当观察到____________,说明瓶内的氧气已收集满。该反应__________(填“能”或“否”)用高锰酸钾制取氧气后的固体剩余物代替二氧化锰作催化剂。
(3)若用装满水的F装置收集氧气,则气体从处导管进入__________(填“a”或“b)。
(4)实验结束后,小王问:“我怎么知道这气体就是氧气?”请你设计实验消除他的疑问:______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知某溶液中的溶质可能是HCl、NaOH、CaCl2中的一种或两种,为确定该溶液中溶质的成分及含量,进行以下实验。
(1)取少量溶液于试管中,滴入2滴无色酚酞试液,酚酞不变色,溶液中一定不存在____。
(2)为了进一步测定成分及含量,重新取120g溶液于烧杯中,逐滴加入20.0%的Na2CO3溶液,测得滴加溶液的质量与产生沉淀的关系(图1)和滴加溶液的质量与烧杯中溶液的pH关系(图2)。 (已知: CaCl2溶液呈中性)回答下列问题

①该溶液中溶质的化学式为_________
②计算溶液中氯化氢的质量分数_______。(写出计算过程)
③m1=_____ g;m2= ____g.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某兴趣小组对氯酸钾(KClO3)分解反应的催化剂进行研究,在相同的加热条牛下,用下图装置完成表中实验:
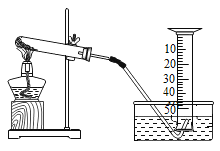
编号 | KClO3质量/g | 催化剂 | 催化剂质量/g | 收集50mLO2所需时间/s。 |
实验1 | 5 | --- | --- | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)编号实验2中5克氯酸钾完全分解后,MnO2的质量为________。
(2)表中所列3种催化剂的催化效果最佳的是___________。
(3)要比较KClO3分解反应中不同催化剂的催化效果,除了测量收集50mLO2所需时间外,还可以测量相同时间内_____________。
(4)氯酸钾在加热的条件下发生分解反应,生成氯化钾与氧气,请写出编号实验2的KClO3分解的化学方程式:____________。
(5)由实验1和实验4可知,KCl_______(填“有”或“无”)催化作用。维持加热条件不变,用实验1再继续收集收集50mLO2,所需时间明显少于171s,解释原因:___________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】向某盐酸和氯化镁的混合溶液中加入某浓度的氢氧化钠溶液,产生沉淀的质量与加入氢氧化钠溶液的质量关系如图所示。
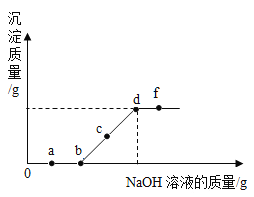
(1)a点溶液中滴入紫色石蕊试液,观察到_____。
(2)bc段(不含b点)反应的化学方程式为_____。基本反应类型为_____。
(3)c点溶液中主要存在的阳离子为_____。
(4)溶液中NaCl的溶质质量分数:d_____f(填“>”“<”或“=”)。
(5)d点溶液中溶质为_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为测定空气中氧气的含量,小华同学打算设计如下图所示的实验方案:
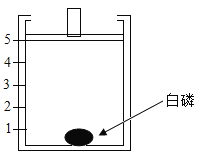
在一个隔热效果良好的容器上方安装一个可自由上下移动的活塞(活塞质量忽略不计起始位置在5刻度处)。加热容器,使容器温度达到80℃(已知白磷燃烧所需的最低温度为40℃)。请回答:
(1)实验过程中,可以观察到:活塞先向_____移动,再向_____移动,最后停在刻度_____处。
(2)由此实验得出的结论_____。
(3)有位同学用木炭取代白磷来进行实验,结果实验失败,请你分析的原因是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com