
分析 Ⅰ、氢氧化钙和稀盐酸反应生成氯化钙和水;
Ⅱ、根据反应物是否过量可以判断溶液中溶质的组成;
显碱性的溶液能使酚酞试液变红色;
碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,和氯化钙反应生成碳酸钙沉淀和氯化钠;
显酸性的溶液pH小于7,能使石蕊试液变红色;
碳酸钙能和稀盐酸反应生成氯化钙、水和二氧化碳.
解答 解:Ⅰ、氢氧化钙和稀盐酸反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O.
故填:Ca(OH)2+2HCl═CaCl2+2H2O.
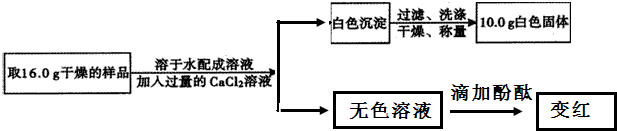
Ⅱ、该烧杯内溶液中的溶质可能是CaCl2和Ca(OH)2;可能只有CaCl2;可能是CaCl2和HCl;
【进行实验】取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡,
实验现象:酚酞试液不变色,
结论:猜想一不正确.
实验步骤取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量,
实验现象:先产生气泡,后产生沉淀,
结论:猜想二不正确,猜想三正确.
【反思与拓展】
(1)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物是否过量;
(2)a.利用pH试纸可以测定溶液的pH,从而可以判断溶液中是否含有稀盐酸,该选项可以;
b.铜不能和稀盐酸反应,该选项不可以;
c.利用紫色石蕊溶液是否变成红色,可以判断溶液中是否含有稀盐酸,该选项可以;
d.硝酸银能和氯化钙反应生成白色沉淀氯化银,因此该选项不可以;
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是腐蚀下水道,酸化水等;
要处理烧杯内溶液,使其溶质只含有CaCl2,应向烧杯中加入过量的不溶于水的碳酸钙.
故填:可能是CaCl2和HCl;酚酞试液不变色;先产生气泡,后产生沉淀;反应物是否过量;ac;腐蚀下水道;碳酸钙.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
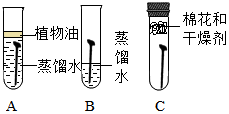 小林同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图.经过一周观察:试管A 和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.根据上述描述请你完成:
小林同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如图.经过一周观察:试管A 和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.根据上述描述请你完成:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
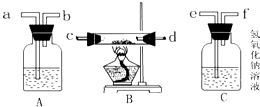
| A. | 甲做完实验后,将剩余的试剂倒回原试剂瓶 | |
| B. | 乙在点燃酒精灯时,用燃着的酒精灯引燃另一只酒精灯 | |
| C. | 丙在取稀盐酸时,在无用量说明的情况下,量取了1-2mL | |
| D. | 丁直接用手将粉末状药品加入试管中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
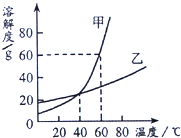
| A. | 40℃时,甲和乙物质的溶解度相同 | |
| B. | 升高温度可使不饱和的甲溶液变为饱和 | |
| C. | 60℃时,溶液甲的浓度大于乙 | |
| D. | 甲的溶解度大于乙的溶解度 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
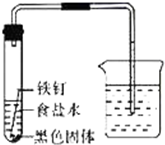 某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图,装置气密性良好),一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.| 实验步骤 | 实验现象 | 实验结论 |
| 你选用的试剂是: 稀盐酸(或稀硫酸) | 有气泡产生(无气泡产生) | 含有铁(不含有铁) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com