
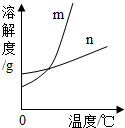
 为探究固体A、B在水中的溶解情况,小明同学实验如下:取两支试管,分别加入一定质量的粉末A和粉末B(A、B均不与水反应),然后逐渐加入适量的水充分振荡并观察记录实验数据,得到了如图所示的图象(横坐标表示水的质量,纵坐标表示溶质的质量).
为探究固体A、B在水中的溶解情况,小明同学实验如下:取两支试管,分别加入一定质量的粉末A和粉末B(A、B均不与水反应),然后逐渐加入适量的水充分振荡并观察记录实验数据,得到了如图所示的图象(横坐标表示水的质量,纵坐标表示溶质的质量). 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题
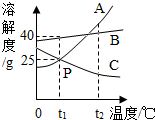 溶液在生产和生活中有重要意义.如图是A、B、C三种固体物质的溶解度曲线,则下列判断正确的是( )
溶液在生产和生活中有重要意义.如图是A、B、C三种固体物质的溶解度曲线,则下列判断正确的是( )| A. | t1℃时,A、B、C三种物质的溶液浓度从大到小的关系是B>A=C | |
| B. | A的不饱和溶液可通过升温、蒸发、添加溶质的方式变为饱和 | |
| C. | t2℃时,等质量的饱和A、B、C溶液降温至t1℃,A析出晶体最多 | |
| D. | A的浓溶液中含有少量C的时候,可用加热蒸发结晶的方式提纯A |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 KNO3和KCl在不同温度时的溶解度如表所示.请回答下列问题:
KNO3和KCl在不同温度时的溶解度如表所示.请回答下列问题:| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 浓硫酸具有吸水性,所以可以做某些气体的干燥剂 | |
| B. | 患胃酸过多症的病人可口服含有NaHCO3或Al(OH)3的药物缓解胃酸过多 | |
| C. | 酸碱生成盐和水的反应,既是中和反应,又属复分解反应 | |
| D. | 稀释浓硫酸时一定要将水慢慢注入浓硫酸中 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | 苯 | 氧气 | 二氧化碳 | 水 | X |
| 反应前质量/g | 3.9 | 9.6 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 6.6 | 2.7 | m |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 25℃时,氢氧化钠沉淀的pH范围 | |||
| Fe(OH)3 | Al(OH)3 | Mg(OH)2 | |
| 开始沉淀的pH | 1.5 | 3.3 | 10.4 |
| 沉淀完全的pH | 3.2 | 5.2 | 12.4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | K2MnO4、MnO2 | B. | KMnO4、MnO2 | ||
| C. | KMnO4、K2MnO4、MnO2 | D. | KMnO4、K2MnO4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com