
【题目】国家质量标准规定,市场出售尿素[CO(NH2)2]中,尿素含量在96%以上为达标一级品,某经销商出售一批尿素,其含氮量为45%,通过计算说明这批尿素是否可按一级品尿素出售?
科目:初中化学 来源: 题型:
【题目】工业上用甲和乙反应制备丙和丁,其反应的微观示意图如下:
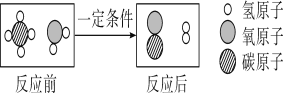
(1)该化学变化中没有发生改变的粒子是_______(填“分子”或“原子”)
(2)写该反应的化学方程式__________________。
(3)该反应中含氢元素的化合物有_____种;反应前后化合价发生了变化的元素是________(填元素符号)。
(4)反应物和生成物中属于氧化物的有____ 种,生成物中____ (填“有”或“没有”)单质。
(5)该化学反应的微观实质是_____________________ 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列说法完全正确的是
A. | 氖气的化学式 — Ne2 1个硅原子 — Si 1个钠离子 —— | B. | 决定元素种类——质子数 决定元素的化学性质——最外层电子数 决定元素周期表元素排列顺序——质子数 |
C. | 铁——由分子构成 二氧化碳——由原子构成 氯化钠——由离子构成 | D. | 分子——化学变化中的最小粒子 原子——保持物质化学性质的最小粒子 离子——带电的原子 |
A. A B. B C. C D. D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】蔗糖(C12H22O11)是一种常用的食品甜味剂。下列关于蔗糖的说法正确的是( )
A. 蔗糖是由碳、氢、氧三种元素组成
B. 蔗糖中含有45个原子
C. 蔗糖中氢元素的质量分数最高
D. 蔗糖的相对分子质量为342g
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请你阅读下列文字和图片,回答问题:臭氧,化学式为O3,有鱼腥气味的淡蓝色气体。有水存在时臭氧是一种强力漂白剂。用作强氧化剂漂白剂、皮毛脱臭剂、空气净化剂,消毒杀菌剂,饮用水的消毒脱臭。液态臭氧还可用作火箭燃料的氧化剂。存在于大气中,靠近地球表面浓度为0.001~0.03ppm,是由大气中氧气吸收了太阳的波长小于185nm紫外线后生成的,臭氧层可吸收太阳光中对人体有害的短波(30nm以下)光线,防止这种短波光线射到地面,使人类免受紫外线的伤害。
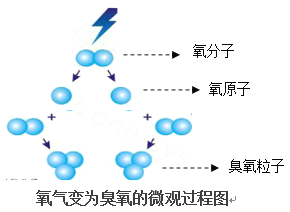
(1)臭氧的物理性质有(答一条):__________________
(2)氧气变成臭氧属于_______________(填“物理”或“化学”)变化
(3)从微观角度看,臭氧是由_________(填“分子”或“原子”)构成。一个构成臭氧的微粒中,质子数为____________,电子数为_____________。
(4)为了防止臭氧层被破坏,我们可以怎么做?(答一条)_____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在宏观、微观和符号之间建立联系是化学学科的特点。
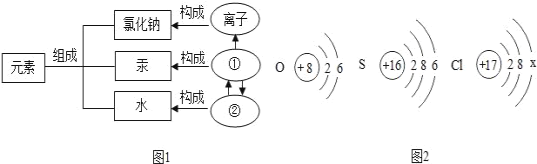
(1)物质的组成及构成关系如图1所示,图中②表示的是_____________(填“分子”或“原子”)。
(2)如图2是氧、硫、氯三种元素的原子结构示意图。
①氯离子的结构示意图中x的数值是___________,其离子符号是__________。
②硫原子在化学反应中易__________电子(填“得到”或“失去”)。
(3)氧和硫两种元素最本质的区别是它们原子中的__________不同。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】海水中蕴藏着丰富的资源,海水“晒盐过程中可得到粗盐和卤水。粗盐中常含有多种杂质,必须对其进行分离和提纯,才能用于生产和生活;卤水经常用作工业制镁的原料。
(1)实验室除去粗盐中不溶性杂质的步骤为:溶解、过滤、蒸发结晶。在三步中都要用到的一种玻璃仪器是____。
(2)若要除去食盐固体中含有的少量CaCl2杂质,得到较为纯净的食盐固体,实验操作步骤为:将食盐固体放入烧杯中,加入足量水溶解,然后向烧杯中先加入过量的____(填化学式)溶液,过滤,再向滤液中加入适量的____(填化学式),最终蒸发结晶。(填化学式)
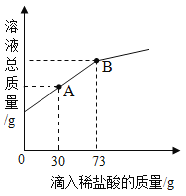
(3)在一烧杯中盛有Mg(OH)2和MgCl2的固体粉末6g,向其中加入20g水,经充分溶解后,再逐滴加入溶质质量分数为10%的稀盐酸。烧杯中溶质的总质量与加入稀盐酸的质量关系如图所示。请回答下列问题。
①当滴入稀盐酸30g时(即图中A点时),烧杯内溶液中的溶质是____(填写化学式)。
②当滴入稀盐酸73g时(即图中B点时),试通过计算,求此温度时所得不饱和溶液中溶质的质量___(计算结果精确至0.1g)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答:

(1)25℃时,将25g甲固体加入到50g水中,充分溶解并恢复到原温度后,得到溶液的质量为 g。
(2)要使35℃时接近饱和的甲溶液变成该温度下的饱和溶液,可采用的一种方法是 。
(3)现有操作步骤: a.溶解 b.过滤 c.降温结晶 d.加热浓缩;若甲固体中含有少量乙,则提纯甲的操作步骤是 (填字母序号)。
(4)将35℃时丙的饱和溶液降温到25℃,则其溶液的溶质质量分数 (填“变大”、“变小”或“不变”)。
(5)向100g35℃的水中加入45g甲固体,发现全部溶解,一段时间后又有部分甲的晶体析出。你认为“全部溶解”的原因可能是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com