
分析 (1)根据氢氧化钠的质量和方程式计算Al2O3的质量,进一步计算铝土矿中Al2O3的质量分数
(2)根据质量守恒分析加入的NaOH溶液中水的质量.
解答 解:(1)设Al2O3的质量为x
Al2O3+2NaOH=2NaAlO2+H2O
102 80
x 160kg
$\frac{102}{x}$$\frac{80}{160kg}$
x=204kg
铝土矿中Al2O3的质量分数$\frac{204kg}{340kg}$×100%=60%
(2)加入的NaOH溶液中水的质量1004kg-204kg-160kg=640kg
答:(1)铝土矿中Al2O3的质量分数60%
(2)加入的NaOH溶液中水的质量640kg
点评 本题考查了根据化学方程式的计算,完成此题,可以依据已有的知识进行.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:解答题
 垃圾发电是把各种垃圾收集后,进行分类处理.其中:一是对燃烧值较高的进行高温焚烧,在高温焚烧中产生的热能转化为高温蒸气,推动涡轮机转动,使发电机产生电能.二是对不能燃烧的有机物在缺乏空气的条件下进行腐烂发酵、产生一种气体沼气.距测算,1米3的沼气池一天产生沼气量0.2米3.1米3沼气可以供6口之家三餐的烹饪,可以使3吨的卡车运行3千米,点亮60W电灯工作6小时.
垃圾发电是把各种垃圾收集后,进行分类处理.其中:一是对燃烧值较高的进行高温焚烧,在高温焚烧中产生的热能转化为高温蒸气,推动涡轮机转动,使发电机产生电能.二是对不能燃烧的有机物在缺乏空气的条件下进行腐烂发酵、产生一种气体沼气.距测算,1米3的沼气池一天产生沼气量0.2米3.1米3沼气可以供6口之家三餐的烹饪,可以使3吨的卡车运行3千米,点亮60W电灯工作6小时.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 已知A、B、C、D、E、F、G、H、M、N均为初中化学中常见的物质,其中A、C、D、M、F为氧化物,组成A与C的元素种类相同;H为可溶性碱;固体X在B中充分燃烧可生成无色气体D;E为常用建筑材料的主要成分.各物质之间的相互关系如图所示(部分反应条件和生成物已省略)
已知A、B、C、D、E、F、G、H、M、N均为初中化学中常见的物质,其中A、C、D、M、F为氧化物,组成A与C的元素种类相同;H为可溶性碱;固体X在B中充分燃烧可生成无色气体D;E为常用建筑材料的主要成分.各物质之间的相互关系如图所示(部分反应条件和生成物已省略)查看答案和解析>>
科目:初中化学 来源: 题型:解答题
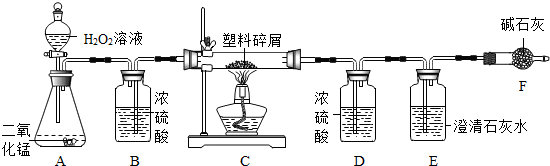
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 水与人类的生活和生产密切相关,请回答下列问题:
水与人类的生活和生产密切相关,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
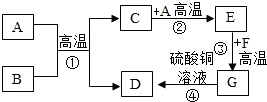 A-H都是初中化学中常见的物质.已知A、B都是黑色固体.D、F为红色固体,它们之间的转化关系如图所示,请回答下列问题:
A-H都是初中化学中常见的物质.已知A、B都是黑色固体.D、F为红色固体,它们之间的转化关系如图所示,请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com