
【题目】用一定量的盐酸完全中和某一强碱溶液,如果改用与盐酸等质量分数、等质量的硝酸,则反应后溶液的pH将会
A.等于0B.等于7C.小于7D.大于7
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
【题目】杂卤石(K2SO4·MgSO4·2 CaSO4·2H2O)属于“呆矿”,为能充分利用钾资源,用饱和的Ca(OH)2溶液浸杂卤石制备硫酸钾,工艺流程如下: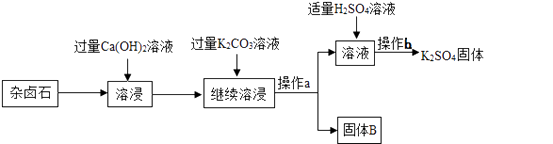
已知:
物质 | CaSO4 | K2SO4 | Mg(OH)2 |
溶解度/g(25℃) | 0.28 | 11.1 | 0.00084 |
(1)操作a的名称为 , 该操作中玻璃棒的作用是_ _。
(2)固体B的主要成分有和。
(3)操作b的步骤是蒸发浓缩、、过滤、洗涤。
(4)在实验流程中加入过量的K2CO3溶液,能除去的物质是;
(5)在使用Ca(OH) 2溶液和K2CO3溶液对杂卤石进行“溶浸”时,为探究获得较高浸出杂卤石主要成分的浸取率,某实验小组用测得浸取液中K+的质量分数来表示浸取率,在相同的时间里,进行了如表实验组:
实验 | 温度/℃ | Ca(OH)2用量/g | K+浸取率/% |
① | 25 | 2.5 | 72.4 |
② | 40 | 2.5 | 86.55 |
③ | 40 | 3 | 90.02 |
④ | 60 | 3 | 91.98 |
⑤ | 60 | 4 | 91.45 |
①上述实验的数据中,温度与K+浸取率的关系是
②如表所列出的5组实验中,若要获得最佳的K+浸取率,选择的反应条件是℃
和g 的Ca(OH) 2用量
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在日常生活和农业生产中,下列物质的用途是由化学性质决定的是( )
A.用活性炭除去冰箱内的异味B.用天然气作燃料
C.用金属铜制作电线D.用金刚石刻划玻璃
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某溶液中仅含有H+、Fe3+、SO4 2-、NO3- 4种离子,已知其中H+、SO4 2-、NO3-的个数比为1︰2︰3,H+的个数是0.2NA,那么Fe3+的个数为
A.1.2NAB.0.4NAC.NAD.0.2NA
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列实验现象叙述错误的是( )
A.镁在空气中燃烧发出耀眼的白光,生成白色固体
B.铁在氧气中燃烧时火星四射,生成黑色固体
C.硫在氧气中燃烧发出淡蓝色火焰
D.一氧化碳在空气中燃烧发出蓝色火焰
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列物质的名称、化学式、俗名一致的是( )
A.氢氧化钙 Ca(OH)2 生石灰B.氢氧化钠 NaOH 苛性钠
C.碳酸铵 NH4HCO3 碳铵D.碳酸氢钠 NaHCO3 纯碱
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究性学习小组为了测定黄铜(铜、锌合金)的组成。在化学老师的帮助下,选用98%的浓硫酸、黄铜样品进行下列实验和计算。
实验Ⅰ:配制150g 9.8%的稀硫酸。
(1)计算:需要浓硫酸的质量g,约8.2mL。
(2)量取:用量筒准确量取所需的浓硫酸和水。
混匀:稀释时一定要将沿器壁慢慢注入里,并不断搅拌。
(3)装瓶贴标签:请填写下侧的标签。
(4)实验Ⅱ:测定黄铜样品中铜的质量分数。称取黄铜样品10g,向其中逐滴加入
9.8%的稀硫酸至刚好不再产生气体为止。反应过程中生成的气体与所用硫酸溶液的质量关系如图所示。
试计算:
样品中铜的质量分数。(计算结果精确到小数点后一位)(在答题卡上写出计算过程)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com