
���� �������еĽ�����֪ʶ���з�����������������ĺϽ������еĺ�̼���ߣ�̼����������Ӧ���ɶ�����̼��̼������������Ӧ�������Ͷ�����̼������������ͭ��Ӧ��������������ͭ����������ʴ�����ؽ���������������ᷴӦ�����Ȼ�����ˮ�����ױ����������������ܵ�����������Ĥ���ݴ˽��
��� �⣺��1�������ĺ�̼���ȸֵĺ�̼���ߣ���������̼�ĺϽ����ڻ�������ߣ�����
��2�����������ȵ�Һ̬���Һ̬�����Ͻ������ʹ���ʳ�ַ�Ӧ�����ʹ���ʳ�ַ�Ӧ��
��3��̼����������Ӧ���ɶ�����̼��̼������������Ӧ�������Ͷ�����̼�����C+O2$\frac{\underline{\;��ȼ\;}}{\;}$CO2��3C+2Fe2O3$\frac{\underline{\;����\;}}{\;}$4Fe+3CO2��
��4������������ͭ��Ӧ��������������ͭ��ʵ�ʲμӷ�Ӧ��������ͭ���ӣ����ɵ����������Ӻ�ͭ�����Fe+CuSO4=FeSO4+Cu��Fe Cu2+��Fe2+ Cu��
��5��������ˮ����������ʱ�����⣬�������������ᷴӦ�����Ȼ�����ˮ�����ױ����������������ܵ�����������Ĥ�����������ˮ��Fe2O3+6HCl�T2FeCl3+3H2O��4Al+3O2=2Al2O3��
���� ���⿼����ǽ������й����ʺ�Ӧ�õ�֪ʶ����ɴ��⣬�����������е�֪ʶ���У�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
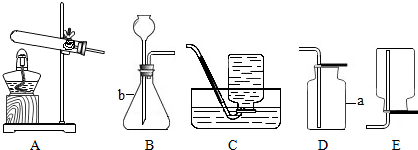
| A�� | 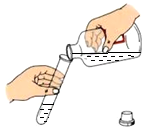 �㵹Һ�� | B�� | 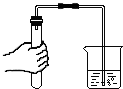 ��������� | ||
| C�� | 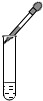 �μ�����Һ�� | D�� | 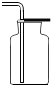 �ռ�������̼���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Mg��Al��Fe | B�� | Fe��Al��Mg | C�� | Al��Mg��Fe | D�� | Mg=Al=Fe |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����õ�ȼ�ķ�����ȥ������̼�л��е�����һ����̼ | |
| B�� | ʯī���������ĵ������ܣ����������缫 | |
| C�� | �Ͻ�Ӳ��һ���������Ĵ������� | |
| D�� | ����粒�������ˮʱ���ȣ����������ƹ�������ˮʱ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 С��������25��ʱ700g KNO3������Һ����֪���¶���KNO3���ܽ��Ϊ40g�������Ĺ������£�
С��������25��ʱ700g KNO3������Һ����֪���¶���KNO3���ܽ��Ϊ40g�������Ĺ������£��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CuCl2��NaOH | B�� | NaCl��AgNO3 | C�� | NaOH��HCl | D�� | NaNO3��HCl |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ˮ�ĵ�� | B�� | ˮ���ܶ� | C�� | ˮ�ķ��ӽṹ | D�� | ˮ��Ԫ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ԭ�ϲ�ͬ | B�� | �õ��IJ�����ȫ��ͬ | ||
| C�� | ��һ��������ѧ�仯 | D�� | ��û�������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com