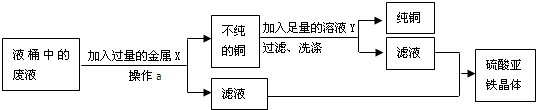
解:(1)由金属活动性顺序表可知:

(2)波尔多液是用硫酸铜和氢氧化钙来配制得到的,反应的化学方程式是:Ca(OH)
2+CuSO
4=CaSO
4+Cu(OH)
2↓;配制时不能用铁制容器,原因是铁能与波尔多液中硫酸铜反应生成了硫酸亚铁和铜,反应的方程式是:Fe+CuSO
4═FeSO
4+Cu.
(3)①Cu与AgNO
3溶液反应,Cu与FeSO
4溶液不反应,能判断三种金属的活动性顺序.故①可选用.
②Fe能与稀硫酸反应,Cu、Ag与稀硫酸不反应,不能比较Cu、Ag的活动性.故②不可选用.
③Cu、Ag不能与FeSO
4溶液反应,无法判断Cu、Ag的金属活动性;故③不可选用.
(4)由Fe 和CuSO
4 溶液反应,说明铁的活动性比铜强;Mg和MnSO
4 溶液反应,说明镁的活动性比锰强;Mn和FeSO
4 溶液反应,说明锰的活动性比铁强;则Mn、Fe、Mg、Cu四种金属活动性由强至弱的顺序为Mg>Mn>Fe>Cu;Mn和FeSO
4溶液反应的方程式是:Mn+FeSO
4=Fe+MnSO
4.
故答为:(1)见上图;(2)Ca(OH)
2+CuSO
4=CaSO
4+Cu(OH)
2↓,Fe+CuSO
4═FeSO
4+Cu.(3)①;(4)Mg>Mn>Fe>Cu;Mn+FeSO
4=Fe+MnSO
4.
分析:(1)根据金属活动性顺序表及意义完成空格;
(2)根据硫酸铜和氢氧化钙的反应、铁与硫酸铜的反应,写出反应的化学方程式;
(3)验证铜、铁、铝三种金属的活动性强弱,一般是利用金属与酸反应或金属与盐溶液的反应,通过金属和酸是否反应或剧烈程度判断金属的活动性,或通过金属是否能和盐溶液发生置换反应判断金属活动性.
(4)根据金属与盐的反应规律,利用Mn、Fe、Mg、Cu四种金属及其化合物间可发生的反应,推断Mn、Fe、Mg、Cu四种金属活动性由强至弱的顺序.
点评:本题考查了常见物之间的反应,完成此题,可以依据已有的金属活动性顺序的应用进行,要求同学们加强基础知识的储备,以便灵活应用.