
分析 (1)根据生铁和钢的成分分析回答;
(2)根据铁在氧气中燃烧生成了四氧化三铁分析回答
(3)根据金属活动性由强到弱的顺序:铁>氢>铜,分析氧化铜中加入稀硫酸发生的反应(CuO+H2SO4=CuSO4+H2O),再加入铁粉可能发生的反应(Fe+CuSO4=FeSO4+Cu、Fe+H2SO4=FeSO4+H2↑),依据实验现象“滤渣A加入足量稀硫酸中,有气泡冒出”,判断发生反应后所得滤渣和滤液的成分.
解答 解:(1)生铁和钢的本质区别是含碳量不同,生铁为2%~4.3%,钢为0.03%~2%.故含碳量较高的是生铁.
(2)铁与氧气在点燃条件下反应生成四氧化三铁.该反应的化学方程式为:3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
(3)根据实验现象“滤渣A加入足量稀硫酸中,有气泡冒出”可知,充分反应后滤渣中含有铁,说明加入的铁是过量的;此时滤液中不存在硫酸和硫酸铜,则所得滤渣中一定含有铜、铁,滤液中一定含有硫酸亚铁.
故答案为:(1)生铁;(2)3Fe+2O2 $\frac{\underline{\;点燃\;}}{\;}$Fe3O4;(3)Cu、Fe;FeSO4、H2O.
点评 体现出了化学中“根据现象,找出原因,判断本质”这一化学理念,考查运用知识分析问题的能力.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 高氯精由4种元素组成 | |
| B. | 高氯精分子中C、O、N、Cl的原子个数比为1:1:1:1 | |
| C. | 高氯精中C、N两种元素的质量比为6:7 | |
| D. | 高氯精是由C、O、N、Cl四种原子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
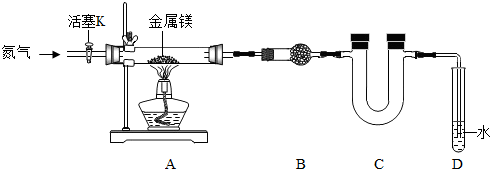
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质 | X | Y | Z | Q |
| 反应前质量/g | 4 | 10 | 1 | 21 |
| 反应后质量/g | 0 | 12 | 15 | 待测 |
| A. | 该反应不可能是分解反应 | |
| B. | 反应后生成14gZ | |
| C. | 参加反应的X与Q的质量比是1:3 | |
| D. | 该反应方程式中X与Q的化学计量数比为3:2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中的CO | 通入O2点燃 |
| B | 除去Zn中混入的少量Fe | 加过量ZnSO4溶液、过滤 |
| C | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、蒸发 |
| D | 鉴别NaCl溶液、Na2SO4溶液和(NH4)2SO4溶液 | 各取少量于试管中,分别滴加Ba(OH)2溶液,观察现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com