
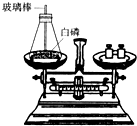
 (1)如图所示为用加热后的玻璃棒点燃白磷,来测定白磷燃烧前后质量的变化情况,用来验证质量守恒定律的实验.
(1)如图所示为用加热后的玻璃棒点燃白磷,来测定白磷燃烧前后质量的变化情况,用来验证质量守恒定律的实验. 4Al+3O2↑对于解答:“电解10t氧化铝最多可生产多少吨铝?”一题,
4Al+3O2↑对于解答:“电解10t氧化铝最多可生产多少吨铝?”一题,| 小倩同学的解法 | 小明同学的解法 |
| 解:设生成的铝质量为X 2Al2O3  4Al+3O2↑ 4Al+3O2↑204108 10t X  = =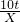 X=5.3t 答:最多可生产5.3t铝 | 解:氧化铝中铝元素的质量分数为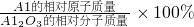  ×100%=53% ×100%=53%铝的质量为10t×53%=5.3t 答:最多可生产5.3t铝 |
 2H2O+O2↑
2H2O+O2↑  =
=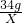


科目:初中化学 来源: 题型:阅读理解
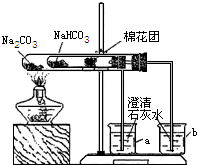 某校同学对市场上的食品疏松剂进行了如下探究.
某校同学对市场上的食品疏松剂进行了如下探究.| 成分 | 所用物质 |
| 碳酸盐类 | 碳酸氢钠 |
| 酸性物质 | 柠檬酸、酒石酸等 |
| 疏松剂 | 明矾 |
| 其他成分 | 淀粉、脂肪酸等 |
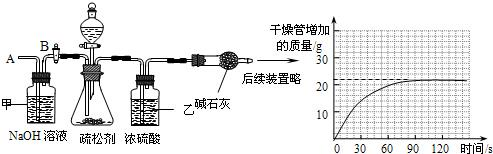
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验步骤和操作 | 实验现象和结论 |
(1)如图所示: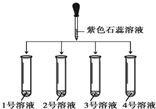 |
①2号溶液由无色变为红色, 则2号溶液是 稀盐酸 ②另三支试管中溶液均由无色变蓝色 |
(2)另取1、3、4号溶液,分别滴加2号溶液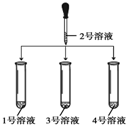 |
①3号溶液中有气泡放出, 则3号溶液是 碳酸钠 ②另外二支试管中溶液无明显变化 |
| (3)另取1,4号溶液,分别滴加 3号溶液 |
①1号溶液中有白色沉淀析出, 则反应的化学方程式为 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH ②另一支试管中溶液中无明显变化 |
| 实验操作 | 实验现象 | 实验结论 |
任取三种溶液于三支试管中,分别滴加第四种溶液 |
①一支试管中有气泡放出 其余二支试管中溶液无明显变化 |
①第四种溶液为稀盐酸 |
| ②一支试管中有白色沉淀析出, 其余二支试管中溶液无明显变化 |
②第四种为Na2CO3溶液 | |
| ③三支试管中溶液均无明显变化 | ③第四种为NaOH溶液 |
| 实验操作 | 实验现象 | 实验结论 |
如图所示: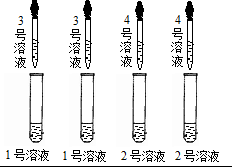 |
①A,B,C均无明显变化 ②D中有沉淀析出 |
标号为1,2,3,4的溶液依次为(用化学式表示): NaOH、Ca(OH)2、HCl、Na2CO3 或HCl、Na2CO3、NaOH、Ca(OH)2 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验步骤和操作 | 实验现象和结论 |
(1)如图所示: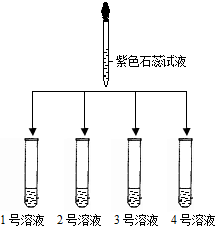 |
①2号溶液由无色变为红色,则2号溶液是 稀盐酸 稀盐酸 ②另三支试管中溶液均由无色变蓝色 |
(2)另取1、3、4、号溶液,分别滴加2号溶液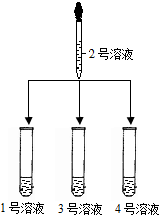 |
①3号溶液中有气泡放出,则3号溶液是 碳酸钠溶液 碳酸钠溶液 ②另二支试管中溶液无明显变化 |
| (3)另取1、4号溶液,分别滴加 碳酸钠溶液 碳酸钠溶液 |
①1号溶液中有白色沉淀析出,则反应的 化学方程式为 Ca(OH)2+Na2CO3=2NaOH+CaCO3↓ Ca(OH)2+Na2CO3=2NaOH+CaCO3↓ ②另一支试管中溶液无明显变化 |
| 实验操作 | 实验现象 | 实验结论 |
| 任取三种溶液 于三支试管中, 分别滴加第四 中溶液 |
一支试管中有气泡放出, 其余二支试管中溶液无明显变化 |
第四种溶液为稀盐酸 |
| 一支试管中有白色沉淀析出, 其余二支试管中溶液无明显变化 |
第四种为碳酸钠溶液 | |
| 三支试管中溶液均无明显变化 | 第四种为氢氧化钠溶液 |
| 实验操作 | 实验现象 | 实验结论 |
(1)如图所示: |
①A、B、C均无明显变化 ②D中有沉淀析出 |
标号为1、2、3、4的 溶液依次为(用化学式 表示): NaOH、Na2CO3、HCl、Ca(OH)2 NaOH、Na2CO3、HCl、Ca(OH)2 或HCl、Ca(OH)2、NaOH、Na2CO3 HCl、Ca(OH)2、NaOH、Na2CO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
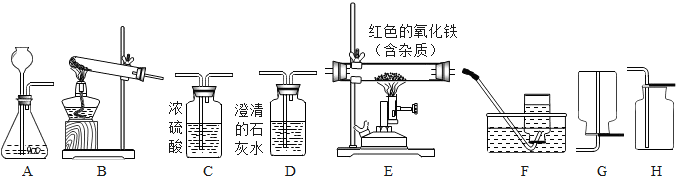
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com