
同学们在实验室进行“粗盐中难溶性杂质的去除”实验。以下是小丽同学的实验报告部分内容。
【实验目的】粗盐中难溶性杂质的去除
【实验过程】
① 用托盘天平称取5.0g粗盐,并全部加入到盛有10mL水的烧杯里,边加边用玻璃棒搅拌;
② 过滤食盐水,观察滤液无色透明;
③ 将所得澄清滤液倒入蒸发皿,加热,并用玻璃棒不断搅拌,当液体蒸干时,停止加热;
④ 用玻璃棒把固体转移到纸上,称量,计算所得精盐的产率。
【实验分析】
(1)步骤①中因为 ,导致实验后精盐产率比其他同学偏低。
(2)步骤③中出现的错误操作是
该操作中玻璃棒的作用
A.加快蒸发速率 B.防止因局部温度过高,造成液滴飞溅 C.引流
【实验反思】经过这样操作所得到的精盐是纯净物吗?
【查阅教材】粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。
【实验设计】
|
实验操作 |
预计实验现象 |
实验结论及解释 |
|
① 将少量所得精盐溶于水,滴加少量稀NaOH溶液 |
|
所得精盐中可能含有氯化镁 化学方程式 |
|
② 取实验①中的上层清液继续滴加NaOH溶液至不再有沉淀时,在上层清液中再滴加 溶液 |
出现白色沉淀 |
所得精盐中可能含有氯化钙 化学方程式 |
【实验结论】除去难溶性杂质得到的精盐不是纯净物。
【实验分析】(1)5.0g粗盐全部加入10mL水中
(2) 不能当液体蒸干时再停上加热(没有等蒸发皿中出现较多固体时再停止热) B
【实验设计】①出现白色沉淀 MgCl2 + 2NaOH = Mg(OH)2 + 2NaCl
②碳酸钠(Na2CO3) CaCl2+Na2CO3==CaCO3↓+2Na Cl
【解析】
试题分析:【实验分析】(1)步骤①中将称取的5.0g粗盐,全部加入到盛有10mL水的烧杯里,粗盐不能全部溶解,则有部分食盐会被过滤掉,所以从食盐水中蒸发所得的精盐的质量偏小,导致实验后精盐产率偏低。
(2)蒸发操作中,当蒸发皿中出现较多固体时要停止加热,利用余热将液体蒸干,故步骤③中出现的错误操作是液体蒸干时,才停止加热;
蒸发操作中,要边加热边搅拌,以防止因局部温度过高,造成液滴飞溅。故选B
【实验设计】①根据实验结论“所得精盐中可能含有氯化镁”可知,将少量所得精盐溶于水,并滴加少量稀NaOH溶液,则NaOH会与其中的MgCl2反应,生成氢氧化镁沉淀和氯化钠,故实验现象为出现白色沉淀,反应的化学方程式为MgCl2+2NaOH=Mg(OH)2 ↓+ 2NaCl。
②取实验①中的上层清液继续滴加NaOH溶液至不再有沉淀时,溶液中不再含有MgCl2,此时再滴加某溶液时,“出现白色沉淀”,再根据实验结论“所得精盐中可能含有氯化钙”可知,滴加的溶液应为碳酸钠溶液,碳酸钠能与氯化钙反应,生成碳酸钙沉淀和氯化钠,故反应的化学方程式为CaCl2+Na2CO3=CaCO3↓+2NaCl。
考点:氯化钠与粗盐提纯,实验探究物质的组成成分
点评:本题主要考查了粗盐提纯的知识和实验探究物质的组成成分,熟练掌握相关基础知识和化学实验基本操作是解答此类题目的关键,关于实验探究物质的组成成分,要熟练掌握相关物质的性质,并能够根据相关反应的现象,对物质的组成做出判断。


 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:
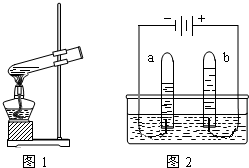 2009年3月22日是“世界水日”.水与人类的生活和生产密切相关.
2009年3月22日是“世界水日”.水与人类的生活和生产密切相关.查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
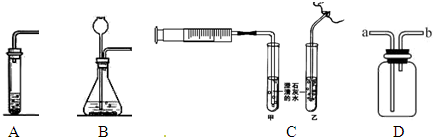
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| 实验操作 | 预计实验现象 | 实验结论及解释 |
| ①将少量所得精盐溶于水,滴加少量稀NaOH溶液 | 出现白色沉淀 出现白色沉淀 |
所得精盐中可能含有氯化镁 化学方程式 MgCl2+2NaOH═Mg(OH)2↓+2NaCl MgCl2+2NaOH═Mg(OH)2↓+2NaCl |
| ②取实验①中的上层清液继续滴加NaOH溶液至不再有沉淀时,在上层清液中再滴加 碳酸钠(Na2CO3) 碳酸钠(Na2CO3) 溶液 |
出现白色沉淀 |
所得精盐中可能含有氯化钙 化学方程式 CaCl2+Na2CO3═CaCO3↓+2NaCl CaCl2+Na2CO3═CaCO3↓+2NaCl |
查看答案和解析>>
科目:初中化学 来源:2013届江苏省南京市鼓楼区中考一模化学试卷(带解析) 题型:探究题
同学们在实验室进行“粗盐中难溶性杂质的去除”实验。以下是小丽同学的实验报告部分内容。
【实验目的】粗盐中难溶性杂质的去除
【实验过程】
① 用托盘天平称取5.0g粗盐,并全部加入到盛有10mL水的烧杯里,边加边用玻璃棒搅拌;
② 过滤食盐水,观察滤液无色透明;
③ 将所得澄清滤液倒入蒸发皿,加热,并用玻璃棒不断搅拌,当液体蒸干时,停止加热;
④ 用玻璃棒把固体转移到纸上,称量,计算所得精盐的产率。
【实验分析】
(1)步骤①中因为 ,导致实验后精盐产率比其他同学偏低。
(2)步骤③中出现的错误操作是
该操作中玻璃棒的作用
A.加快蒸发速率 B.防止因局部温度过高,造成液滴飞溅 C.引流
【实验反思】经过这样操作所得到的精盐是纯净物吗?
【查阅教材】粗盐中含有多种可溶性杂质(氯化镁、氯化钙等)和不溶性杂质(泥沙等)。
【实验设计】
| 实验操作 | 预计实验现象 | 实验结论及解释 |
| ① 将少量所得精盐溶于水,滴加少量稀NaOH溶液 | | 所得精盐中可能含有氯化镁 化学方程式 |
| ② 取实验①中的上层清液继续滴加NaOH溶液至不再有沉淀时,在上层清液中再滴加 溶液 | 出现白色沉淀 | 所得精盐中可能含有氯化钙 化学方程式 |
查看答案和解析>>
科目:初中化学 来源:北京期末题 题型:填空题
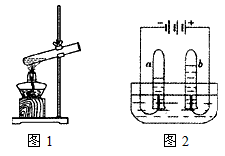
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com