


 同步练习强化拓展系列答案
同步练习强化拓展系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源:2010年全国中考真题专题汇编专题二、物质的鉴别、鉴定、推断3 题型:推断题
(10贵港18)为了回收硝酸亚铁和硝酸银的混合溶液中的银,设计了如下的实验方案: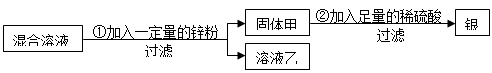
(1)若溶液乙为无色溶液,则固体甲一定有的物质是________,可能有的物质是________,步骤②中肯定发生的反应的化学方程式为________________________________。
(2)若溶液乙为浅绿色溶液,则溶液乙中溶质的组成可能是________________或____________(填物质的名称或化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
为了回收硝酸亚铁和硝酸银的混合溶液中的银,设计了如下的实验方案:
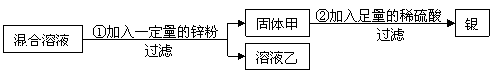
(1)若溶液乙为无色溶液,则固体甲一定有的物质是________,可能有的物质是________,步骤②中肯定发生的反应的化学方程式为________________________________。
(2)若溶液乙为浅绿色溶液,则溶液乙中溶质的组成可能是________________或____________(填物质的名称或化学式)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com