

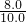 ×100%=80%
×100%=80%

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:
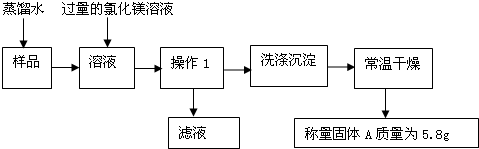
查看答案和解析>>
科目:初中化学 来源: 题型:
| 物 质 | 样 品 | 消耗稀盐酸质量 | 反应后溶液质量 |
| 质量(g) | 9 | 75.4 | 80 |
查看答案和解析>>
科目:初中化学 来源: 题型:
 (2013?闵行区二模)某品牌纯碱中含有少量氯化钠.化学探究小组为了测定该纯碱的纯度(即碳酸钠的质量分数),利用右图装置进行实验测定.
(2013?闵行区二模)某品牌纯碱中含有少量氯化钠.化学探究小组为了测定该纯碱的纯度(即碳酸钠的质量分数),利用右图装置进行实验测定.| 称量项目 | 称量时间 | 质量/g |
| 试样 | 11.0 | |
| 装置+稀盐酸 | 160.0 | |
| 装置+稀盐酸+试样 | 反应开始后20s | 167.0 |
| 装置+稀盐酸+试样 | 反应开始后30s | 166.6 |
| 装置+稀盐酸+试样 | 反应开始后90s | 166.6 |
查看答案和解析>>
科目:初中化学 来源:2011年广东省广州市番禺区中考化学模拟试卷(解析版) 题型:填空题
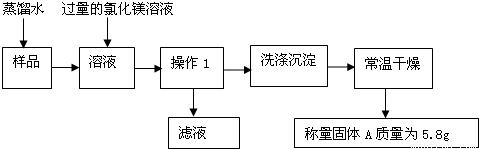
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com