A、B、C、D、E五瓶无色透明溶液,分别是HCl溶液、Na2CO3溶液、MgCl2溶
液、NaNO3溶液、NaOH溶液中的一种.分别进行下列实验:
Ⅰ.将A分别滴入B、C、D、E中,均没有明显现象.
Ⅱ.将B分别滴入A、C、D、E中,C、E中均产生白色沉淀(微溶物也视为沉淀),其余没有明显现象.
Ⅲ.将C分别滴入A、B、D、E中,B中产生白色沉淀,D中有气泡冒出,其余没有明显现象.
(1)A是 ;
(2)B加入E中的化学方程式是 .
【答案】
分析:(1)将五种物质用表格的形式表示出所有的现象,然后对照进行解答.
(2)根据(1)中推出的化学式进行书写方程式
解答:解:(1)将五种物质列表,现象如下,
| | HCl | Na2CO3 | MgCl2 | NaNO3 | NaOH |
| HCl | ------ | 气体 | 无现象 | 无现象 | 无现象 |
| Na2CO3 | 气体 | ------ | 沉淀 | 无现象 | 无现象 |
| MgCl2 | 无现象 | 沉淀 | ------- | 无现象 | 沉淀 |
| NaNO3 | 无现象 | 无现象 | 无现象 | ------ | 无现象 |
| NaOH | 无现象 | 无现象 | 沉淀 | 无现象 | ------- |
根据表格可知,将一种物质分别加入四种溶液中都无现象的是硝酸钠,A为NaNO
3 将B加入到其它四种溶液中,两种溶液中会出现沉淀,两种无现象的是氯化镁,故B为氯化镁;将C分别滴入A、B、D、E四种溶液中,一种产生白色沉淀,一种有气泡冒出,其余没有明显现象,则C为碳酸钠,D为盐酸.故E为氢氧化钠.
(2)氯化镁和氢氧化钠反应生成氯化钠和氢氧化镁沉淀,化学方程式为:MgCl
2+2NaOH═Mg(OH)
2↓+2NaCl
故答案为:(1)NaNO
3(2)MgCl
2+2NaOH=Mg(OH)
2↓+2NaCl
点评:在解此类题时,所给的物质都是无色的,就需要借助表格进行现象列举,然后根据题中的现象进行对照解答



 特高级教师点拨系列答案
特高级教师点拨系列答案 已知:A是相对分子质量最小的氧化物,D是最简单的有机物.请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题.
已知:A是相对分子质量最小的氧化物,D是最简单的有机物.请分析A、B、C、D、E五种物质之间的变化关系,回答有关问题.
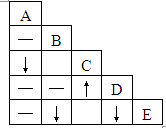 有A、B、C、D、E五瓶失去标签的溶液,各瓶可能是Na2CO3、BaCl2、Ca(NO3)2、稀硫酸、AgNO3溶液中的一种.现将瓶内溶液各取少许,进行部分两两混合的实验,实验结果见如图.说明:表中↑表示有气体生成,↓表示有沉淀生成,-表示无明显现象或有微溶化合物生成,空格表示实验没做.
有A、B、C、D、E五瓶失去标签的溶液,各瓶可能是Na2CO3、BaCl2、Ca(NO3)2、稀硫酸、AgNO3溶液中的一种.现将瓶内溶液各取少许,进行部分两两混合的实验,实验结果见如图.说明:表中↑表示有气体生成,↓表示有沉淀生成,-表示无明显现象或有微溶化合物生成,空格表示实验没做.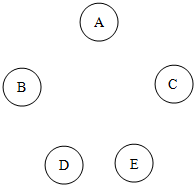 (2013?青岛)现有A、B、C、D、E五种物质,分别为盐酸、硫酸铜、氢氧化钙、铁粉和氧化钙中的一种.其中,A的浓溶液是无色液体,有刺激性气味,在空气中会形成白雾;B为单质;D是“波尔多液”的主要成分之一;E是熟石灰的主要成分.请回答下列问题:
(2013?青岛)现有A、B、C、D、E五种物质,分别为盐酸、硫酸铜、氢氧化钙、铁粉和氧化钙中的一种.其中,A的浓溶液是无色液体,有刺激性气味,在空气中会形成白雾;B为单质;D是“波尔多液”的主要成分之一;E是熟石灰的主要成分.请回答下列问题: