
 甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )
甲、乙两种固体的溶解度曲线如图所示,下列说法正确的是( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 将甲的饱和溶液变为不饱和溶液可采用降温的方法 | |
| C. | t1℃时,甲、乙的饱和溶液中溶质的质量分数不一定相等 | |
| D. | t2℃时,将甲、乙等质量的饱和溶液降温至t1℃,甲析出的固体一定大于乙 |
分析 A、根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
B、饱和溶液和不饱和溶液之间可以相互转化;
C、饱和溶液中溶质的质量分数=$\frac{溶解度}{100g+溶解度}$×100%;
D、根据溶解度曲线、溶液质量可以判断温度变化时析出晶体质量的多少.
解答 解:A、由溶解度曲线可知,温度低于t1℃时,甲的溶解度小于乙的溶解度,该选项说法不正确;
B、由溶解度曲线可知,甲的溶解度随着温度的升高而增大,将甲的饱和溶液变为不饱和溶液可采用升温的方法,降温时仍然是饱和溶液,该选项说法不正确;
C、t1℃时,甲、乙的溶解度相等,其饱和溶液中溶质的质量分数一定相等,该选项说法不正确;
D、t2℃时,甲的溶解度大于乙,t1℃时,甲、乙的溶解度相等,因此将甲、乙等质量的饱和溶液降温至t1℃,甲析出的固体一定大于乙,该选项说法正确.
故选:D.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
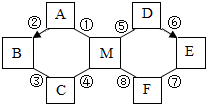 如图所示,它们都是初中化学学习中常见的物质与化学反应“-”表示相连物质能在一定条件下发生化学反应,“→”表示某物质在一定条件下可以生成指向的物质,反应条件都已略去.其中A、B是常见的金属,D、E都是氧化物,反应④、⑦都有白色沉淀生成.请回答下列问题:
如图所示,它们都是初中化学学习中常见的物质与化学反应“-”表示相连物质能在一定条件下发生化学反应,“→”表示某物质在一定条件下可以生成指向的物质,反应条件都已略去.其中A、B是常见的金属,D、E都是氧化物,反应④、⑦都有白色沉淀生成.请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
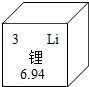 锂电池在手机和电脑中被广泛使用.在元素周期表中,锂元素的信息如图所示,对图中信息解释不正确的是( )
锂电池在手机和电脑中被广泛使用.在元素周期表中,锂元素的信息如图所示,对图中信息解释不正确的是( )| A. | 原子序数为3 | B. | 锂原子的核外电子数为3 | ||
| C. | 元素符号为Li | D. | 锂原子的质量为6.94g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡,直至完全溶解. | 无气泡产生 | 猜想 I不成立 |
| ②取少量①中的溶液于试管中,滴加CaCl2溶液. | 有白色沉淀产生 | 证明有Na2CO3存在 |
| ③ 取少量①中的溶液于试管中,加入过量CaCl2溶液使沉淀完全,静置后,向上层清液中滴加酚酞试液 | 酚酞试液变红 | 证明有NaOH存在 |
综合以上实验现象,说明猜想II是成立的. | ||
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
假设正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
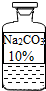 (1)根据图示信息,用化学用语填空:
(1)根据图示信息,用化学用语填空: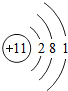
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com