
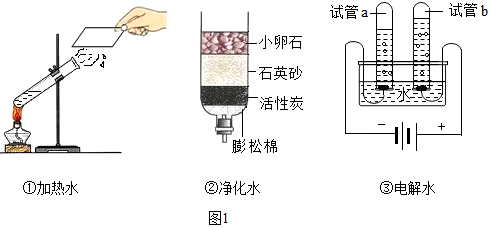
分析 (1)根据活性炭具有吸附性进行解答;纯净物由一种物质组成,混合物由两种或两种以上的物质组成;
(2)电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2;
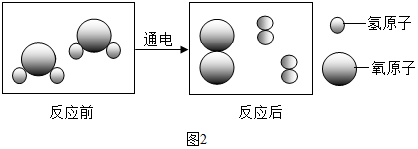
(3)化学反应前后,元素的种类不变,原子的种类、总个数不变;
(4)化学变化中分子能够再分,物理变化中分子不能再分;
(5)能确认水是由氧元素和氢元素组成的实验要根据质量守恒定律进行分析解答.
解答 解:(1)由于活性炭具有吸附性,在简易净水器(图1所示)净化池塘水时,其中活性炭的作用是吸附作用.
净化后的池塘水中含有水和一些溶于水的物质,属于混合物;
矿泉水中含有水和一些溶于水的矿物质,属于混合物;
蒸馏水中含有一种物质--水,属于纯净物;
自来水中含有水和一些溶于水的物质,属于混合物.
(2)实验③中通电一段时间后,试管a中气体较多,是氢气;试管b中气体的气体是O2,试管a、试管b中气体的体积比约为2:1;该实验说明水是由氢元素和氧元素组成的,反应的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
(3)由于化学反应前后原子的种类、总个数和质量都没有发生变化,因此在化学反应中质量守恒.
(4)从微观角度分析,实验①和③两个变化中最本质的区别是电解水时水分子发生改变,蒸发水时水分子没有改变.
(5)能确认水是由氧元素和氢元素组成的实验要根据质量守恒定律,反应前后元素种类不变,氢气在氧气中燃烧生成水和水通电生成氧气和氢气,都能说明水中含有氢元素和氧元素.
答案:
(1)吸附异味和色素; 蒸馏水;
(2)2:1;O2;2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
(3)种类; 数目;
(4)①中只是水分子的空隙变大,③中水分子变为氢分子和氧分子.
(5)AD
点评 本题为涉及水的电解、净化等基础知识,题目难点不大但涉及面较广,耐心审题、沉着作答.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.实验方法 | B.化学与生活 |
| ①鉴别N2、CO2--用燃着的木条 ②熄灭酒精灯--用嘴吹灭 ③除去铁锈--用稀盐酸 | ①世卫组织推广使用中国铁锅预防贫血症 ②地壳中含量最多的非金属元素是氧元素 ③进入久未开启的菜窖之前做灯火试验 |
| C.实验记录 | D.物质构成 |
| ①用10mL烧杯量取4.8mL水 ②20mL水与20mL酒精混合体积小于40mL ③用托盘天平称取5.6g食盐 | ①空气、液氧、二氧化碳中都含氧分子 ②原子都是由质子、中子和电子构成的 ③铁、铜、汞等金属由原子构成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| I | 50.0g | 1% | 0.1g | 9mL |
| II | 50.0g | 2% | 0.1g | 16mL |
| III | 50.0g | 4% | 0.1g | 31mL |


| 步骤③现象 | 步骤⑥结果 | 步骤⑦操作 | 结论 |
| 有大量气泡产生,带火星的木条复燃; | 固体质量仍为0.2g; | 将固体加入盛有5mL5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象. | 在过氧化氢溶液的分解反应中,氧化铜也能作催化剂. |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 称量项目 | 甲 | 乙 | 丙 |
| 所取样品的质量/g | 15 | 15 | 20 |
| 加入氯化钡溶液的质量/g | 150 | 100 | 100 |
| 反应后所得沉淀的质量/g | 23.3 | 23.3 | 23.3 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com