


科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
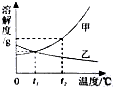 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.查看答案和解析>>
科目:初中化学 来源:2013-2014学年重庆市九年级3月月考化学试卷(解析版) 题型:填空题
实验室提供了①天平②量筒③烧杯④玻璃棒⑤酒精灯等仪器,小华同学用固体氯化钠配制10%的氯化钠溶液,小明同学用固体氢氧化钠配制10%的氢氧化钠溶液,小亮同学用浓盐酸配制10%的稀盐酸。
(1)小华同学配制过程中用玻璃棒搅拌是为了???????????????????? 。
(2)小明用量筒量取水时俯视读数,则所配氢氧化钠溶液溶质质量分数?????? 10%(填“大于”、“小于”或“等于”)。
(3)小亮同学配制10%的稀盐酸的步骤有:①稀释②计算③装瓶并贴标签④量取浓盐酸和水。其正确的顺序为?????? (填序号)。
(4)上述仪器中,三位同学都不需要的仪器是?????? (填序号,后同)小华和小明需要而小亮不需要的仪器是????????????? 。
(5)他们忘记了给配制的三瓶溶液贴上标签,想对未贴标签的三瓶溶液进行鉴别。请你帮
助他们选出可以将三瓶溶液鉴别出来的试剂????????????? 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com