
【题目】10月9日,2019年诺贝尔化学奖正式揭晓。约翰·古德诺、斯坦利·惠廷汉姆和吉野彰因为在锂电子电池研发领域做出的贡献而获奖。如图是元素周期表中锂元素的信息,下列说法中错误的是( )
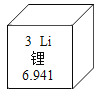
A.锂元素是一种非金属元素
B.锂原子核内有3个质子
C.锂元素的相对原子质量是6.941
D.锂元素组成单质的化学式为Li
科目:初中化学 来源: 题型:
【题目】治疗H1N1流感病毒的良药的主要原料是莽草酸,如图为莽草酸理化性质的描述.回答下列问题:

①莽草酸物质中,共有3种元素,其中氢、氧两种元素的质量比为_____;
②其中属于化学性质的是_____(填图中序号);
③87克莽草酸中含碳元素的质量是_____g.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】芯片的基材主要是高纯硅。如图是一种制备高纯硅的工艺流程图:
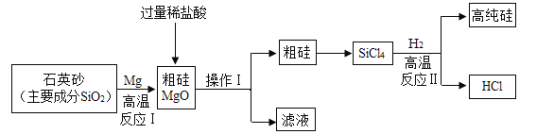
[查阅资料]常温下,氯化镁溶液呈中性
(1)操作I的名称是_________,该操作使用到的玻璃仪器有:玻璃棒、烧杯和___________。
(2)反应I的化学方程式:2X+SiO2![]() Si+2MgO,其中X为:___________(填化学式);SiO2中Si元素的化合价为___________;
Si+2MgO,其中X为:___________(填化学式);SiO2中Si元素的化合价为___________;
(3)写出反应II的化学方程式____________该反应属于_______________(填基本反应类型);该反应要在无氧的环境中进行,原因是_______(答出一种即可)
(4)上述已知生产流程中,可以循环利用的物质是____________(填化学式)。
(5)简要叙述检验盐酸已过量的方法_________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
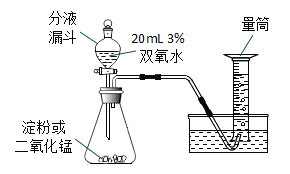
【题目】已知淀粉也能做过氧化氢分解的催化剂。为了比较淀粉与二氧化锰的催化效果,某小组设计了如下实验。实验均以生成25mL气体为准,其他可能的影响因素忽略不计。相关数据如下表:
实验编号 | 3%过氧化氢溶液的体积 | 催化剂质量 | 待测数据 |
Ⅰ | 20mL | 淀粉0.5g | a |
Ⅱ | 20mL | 二氧化锰0.5g | b |
请回答:
(1)该实验中的自变量是________,实验中不采用排空气法收集氧气的原因是_______。
(2)测量氧气的体积时,如果仰视读数,则测量结果______(填“大于”、“小于”或“等于”)实际体积。最后结果表明二氧化锰的催化效果更好,则a____b(填“<”、“>”或“=”)。
(3)小明将光亮的红色的铜丝放在酒精灯火焰上灼烧至表面变黑后,迅速伸入一只装有20mL3%过氧化氢溶液的试管里,试管内立即产生大量气泡。小明据此得出结论:氧化铜可以加快过氧化氢的分解速率。有同学认为该结论不可靠,原因是过氧化氢分解速率加快还可能与_______有关。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化氢(H2O2)广泛应用于纺织、医药、卫生行业,常作漂白剂和消毒剂。
(1)过氧化氢与_________(填物质名称)组成元素相同。
(2)过氧化氢中氧元素的化合价是______________。
(3)向盛有硫酸和高锰酸钾稀溶液的试管中加入足量过氧化氢溶液,发生下列反应: 5H2O2+2KMnO4+3H2SO4=K2SO4+2MnSO4+8H2O+5_______↑。
为检验生成的气体,应进行的操作是__________。
(4)请将下图反应后的物质微观示意图补充完整,要求能体现质量守恒定律。_________
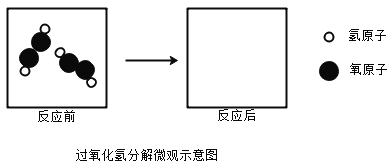
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】气压传感器可用于检测密闭体系内的气压变化,并以数字、曲线等多种形式形象地显示出来。图1为空气中氧气含量测定的实验装置。连接好实验装置,将气压传感器接入电脑并打开,点燃燃烧匙内的足量红磷并塞入集气瓶,集气瓶内气压一时间关系如图2所示。
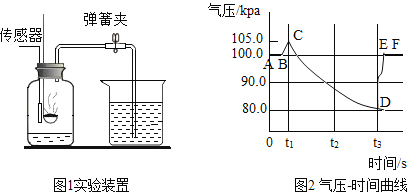
(1)图1实验需要足量的红磷,请写出反应的文字表达式_________________。
(2)图2中CD段气压变化的原因是________________,t3时刻DE段气压又显著增加,因为进行了一个实验操作,即__________________。
(3)实验中,有两个现象都可以得出氧气约占空气体积的![]() 的结论,请写出图1的现象_______________。
的结论,请写出图1的现象_______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氰氨基化钙(CaCN2)是一种重要的化工原料,制备CaCN2的化学方程式为CaCO3+2X=CaCN2+CO↑+H2↑+CO2↑.该反应中下列说法正确的是( )
A. 可用氢氧化钠溶液处理有害的气体产物B. 反应后气体质量减少
C. X的化学式为HCNOD. X溶液的![]()
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请用化学用语填空:
(1)氯原子___;(2)氧化亚铁中铁元素的化合价___;
(3)3个镁离子___;(4)碘酒的溶剂___;
(5)焊接金属时常用作保护气的是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国科学家侯德榜创立候氏制碱法为纯碱和化肥工业的发展做出了杰出贡献。下图1是候氏制碱法的反应原理,图2是相关物质的溶解度曲线,请结合图示回答下列问题:
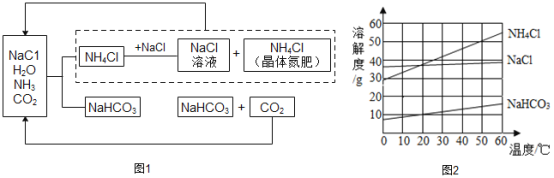
(1)制碱的主要反应原理:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3,生成的碳酸氢钠和氯化铵哪种物质首先析出?_______;理由是_______;
(2)该过程中除水外.能够循环利用的物质是_______;
(3)写出NaHCO3→Na2CO3 反应的化学方程式____________;
(4)50°C时,向100g水中加入55g氯化铵充分搅拌,所得溶液为____(填“饱和”或“不饱和”)溶液;
(5)60°C时,向等质量的氯化钠、碳酸氢钠、氯化铵中,分别加人水配成饱和溶液,所得溶液的质量由小到大的顺序是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com