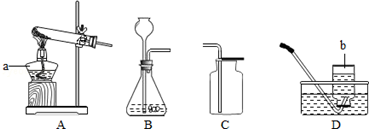
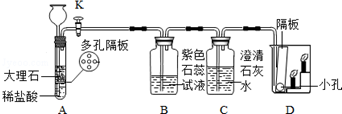
解:(1)熟悉常见的仪器①是试管,结合仪器的用途---收集气体确定②是集气瓶,故答案为:①是试管,②是集气瓶;
(2)实验室用高锰酸钾制取氧气,为了防止高锰酸钾粉末进入导气管,装置A还需做的一点改动是在试管口塞一团棉花,根据化学方程式的书写步骤,加热高锰酸钾制取氧气的反应原理是:2KMnO
4 
K
2MnO
4+MnO
2+O
2↑.故答案为:①需在试管口塞一团棉花,②2KMnO
4 
K
2MnO
4+MnO
2+O
2↑;
(3)①根据化学方程式的书写步骤,铁丝在氧气中燃烧的化学方程式为:3Fe+2O
2 
Fe
3O
4;
②由于铁丝燃烧的条件比较苛刻,根据铁丝在氧气中燃烧的实验,没有观察到“剧烈燃烧,火星四射”的现象的原因可能是:铁丝已经生锈;收集的氧气不纯;而集气瓶中没装水,产生的后果可能是集气瓶炸裂.故答案为:①3Fe+2O
2 
Fe
3O
4,A、B;
(4)①根据信息提供制取二氧化碳的反应物的状态和反应的条件确定发生装置属于“固体加热”型,发生装置应选 A;②利用碳酸氢铵分解出二氧化碳的同时,又产生氨气,因此不便于将两者分离,无法收集到纯净的二氧化碳.故答案为:A,碳酸氢铵加热后产生两种气体,无法收集到纯净的二氧化碳.
故答案为:(1)①是试管,②是集气瓶;(2)①需在试管口塞一团棉花,②2KMnO
4 
K
2MnO
4+MnO
2+O
2↑;(3)①3Fe+2O
2 
Fe
3O
4,A、B;(4)A,碳酸氢铵加热后产生两种气体,无法收集到纯净的二氧化碳.
分析:(1)认识常见的化学仪器;
(2)根据实验室用高锰酸钾制取氧气的原理及注意事项分析;
(3)根据铁丝燃烧的现象及注意事项分析;
(4)根据信息提供制取二氧化碳的反应物的状态和反应的条件确定发生装置,并从产物的特点是两种气体分析不选的原因.
点评:解答本题的关键是要掌握气体的实验室制法中有关反应原理、发生装置和实验操作注意事项等方面进行比较以及归纳铁在氧气中燃烧的条件方面的分析,及化学方程式书写的方法等.


 Na2CO3+H2O+CO2↑ ②NH4HCO3
Na2CO3+H2O+CO2↑ ②NH4HCO3 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑ K2MnO4+MnO2+O2↑.故答案为:①需在试管口塞一团棉花,②2KMnO4
K2MnO4+MnO2+O2↑.故答案为:①需在试管口塞一团棉花,②2KMnO4  K2MnO4+MnO2+O2↑;
K2MnO4+MnO2+O2↑; Fe3O4;
Fe3O4; Fe3O4,A、B;
Fe3O4,A、B; K2MnO4+MnO2+O2↑;(3)①3Fe+2O2
K2MnO4+MnO2+O2↑;(3)①3Fe+2O2  Fe3O4,A、B;(4)A,碳酸氢铵加热后产生两种气体,无法收集到纯净的二氧化碳.
Fe3O4,A、B;(4)A,碳酸氢铵加热后产生两种气体,无法收集到纯净的二氧化碳.

 阅读快车系列答案
阅读快车系列答案