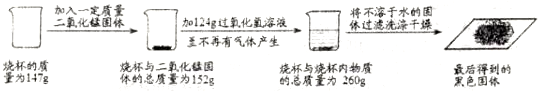
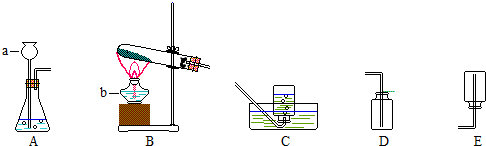
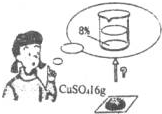
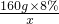解:(1)图示是配制溶液的问题,过程是利用16g硫酸铜配制8%的硫酸铜溶液,可设计如下实际问题:为了检验糖尿病患者的尿液.医院要配制8%的CuSO
4 溶液.现有16gCuS0
4固体.可配制8%的CuSO
4溶液多少克?
(2)因为配制前后溶质的质量不变,所以设可配制8%的CuSO
4溶液质量是x,则有x×8%=16g,解得x=200g;
(3)溶液的配制一般需要经过①计算 ②量取 ③溶解(或配制溶液),由(2)的计算可知溶液的质量是200g,则配制时水的质量是200g-16g=184g,因此配置的步骤是:①计算知需水184g,②用量筒量出184ml水(水的密度是1g/ml),并将其倒入烧杯中③将16g硫酸铜放入到盛有184ml水的烧杯中搅拌溶解,既得溶解8%的CuSO
4溶液;
(4)设生成沉淀的质量是X
CuSO
4+2NaOH=Cu(OH)
2↓+Na
2SO
4160 98
160g×8% x
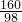
=
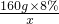
x=7.84g
故答案为:(1)为了检验糖尿病患者的尿液.医院要配制8%的CuSO
4 溶液.现有16gCuS0
4固体.可配制8%的CuSO
4溶液多少克?
(2)答:可配制8%的CuSO
4溶液质量是200g;
(3)①计算知需水184g,②用量筒量出184ml水(水的密度是1g/ml),并将其倒入烧杯中③将16g硫酸铜放入到盛有184ml水的烧杯中搅拌溶解,既得溶解8%的CuSO
4溶液;
(4)答:生成沉淀的质量是7.84g.
分析:(1)从图示数据分析有16g硫酸铜配置8%的硫酸铜溶液进行编制即可.
(2)依据配置前后溶质的质量不变分析解决;
(3)从配置溶液的步骤计算、称量溶解三步完成配置;
(4)根据溶液的有关计算求出硫酸铜溶液中的硫酸铜质量,然后利用方程式的计算列出比例式求出氢氧化铜的质量即可;
点评:本题是溶液配置的方法归纳,是自编溶液的计算,是利用溶液中各种量的关系解决问题.充分体现了开放性、自主性,是对学生思考问题的方法和思考、解决问题的过程和考核促进学生从“学会”向“会学”转变

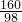 =
=