
【题目】我国化学家侯德榜发明了联合制碱法,其生产纯碱的产品和副产品氯化铵的工艺流程如图所示:
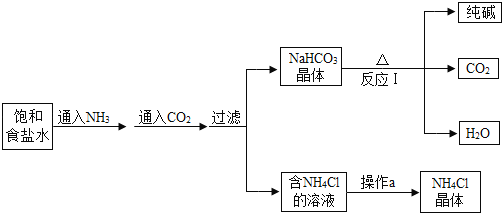
(1)NH3溶于水得到氨水,将无色酚酞溶液滴入氨水中,溶液呈 色.
(2)写出反应I的化学方程式 ;该反应的基本类型为 .
(3)操作a的过程是蒸发浓缩、 、过滤.
(4)上述工艺流程中可循环利用的物质是 .
 全程金卷系列答案
全程金卷系列答案 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:初中化学 来源: 题型:
【题目】阅读下面科普短文。
酸奶营养丰富,富含人体生长发育所必须的多种营养物质,是人们喜爱的食品。
表 1 某品牌酸奶中主要营养成分的含量(每 100 克)
蛋白质/克 | 糖类/克 | 脂肪/克 | 钠/毫克 | 钙/毫克 |
2.7 | 9.5 | 2.7 | 75 | 90 |
但是,普通酸奶含有乳糖,经调查,我国有 88.9%的成人缺乏分解乳糖的乳糖酶,有55.1%的成年人表现有乳糖不耐受症状(主要症状为腹泻)。因此,在保证普通酸奶基本营养不损失的前提下,乳糖含量较低或无乳糖的酸奶成为乳糖不耐受消费者的需求。相关科研技术人员为满足消费者的需求,开始研发无乳糖酸奶。无乳糖酸奶的工艺流程为:原料乳 → 标准化 → 添加 6%的白砂糖 → 均质 → 巴氏杀菌 → 冷却→接种发酵剂(直投式发酵剂)→ 发酵(37℃、42℃)→ 4℃低温储存。
研究一 发酵酸奶中添加乳糖酶对乳糖水解效果的影响
在 37℃,向普通酸奶中添加不同剂量乳糖酶(剂量分别为 1000U/kg、1500U/kg、2000U/kg、2500U/kg),发酵 3 小时,测得发酵酸奶中乳糖残留量随时间的变化,如图 1 所示。
研究二 普通酸奶和无乳糖酸奶发酵过程中的酸度变化
普通酸奶和无乳糖酸奶分别在 37℃和 42℃发酵 8 小时,发酵过程中酸度(从 1 小时开始测量)变化如图 2 所示。
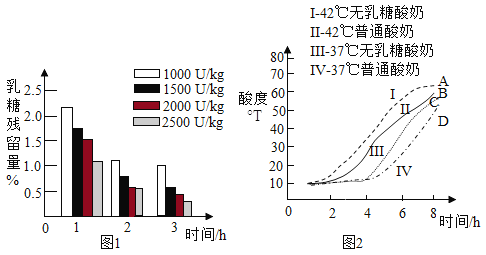
除以上研究,科技人员还在口味、活菌数、保存等方面做了无乳糖酸奶与普通酸奶的对比研究,发现无乳糖酸奶都具有一定的优势。
依据文章内容回答下列问题。
(1)由表 1 可知酸奶的主要营养成分中含量最高的是_______。
(2)由图 1 可知:3 小时内,_______(填字母序号,下同)。
A添加相同量乳糖酶,发酵酸奶中乳糖残留量随时间的延长而降低
B相同发酵时间,乳糖残留量均随乳糖酶添加量的增大而降低
C乳糖残留量与温度、时间、乳糖酶添加量有关
(3)由图 2,影响无乳糖酸奶酸度的因素是_______。
(4)由图 2 可知:42℃时无乳糖酸奶发酵过程中酸度与时间的关系是_______。
(5)下列说法正确的是_______。
A我国绝大部分成年人都有乳糖不耐受症状
B表 1 中“钠”指的是钠元素
C无乳糖酸奶的工艺中至少两步属于化学变化
D无乳糖酸奶比普通酸奶适合更多消费者食用
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】物质王国举行一场趣味篮球赛。某队由铁、二氧化碳、硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成一次有效进攻。场上“队员”位置及传球路线如图所示。
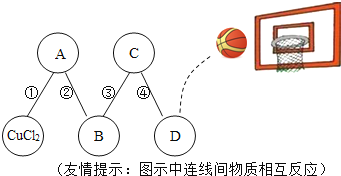
(1)已知D位置上投篮的“队员”是个灭火“能手”,则D位置“队员”代表的物质是________;
(2)B位置“队员”所代表物质的一种用途是________;
(3)写出连线④代表的物质间发生反应的化学方程式________;连线①代表的物质间发生化学反应的基本类型是________反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学活动小组以“酸碱盐的性质”为主题进行探究性学习,请你作为该小组成员一起来解决下列问题:
(1)小红同学用下图总结了 NaOH 的四条化学性质(即 NaOH 与四类物质能够发生化学反应)。
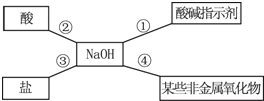
依据上图反应④说明 NaOH 必须密封保存,否则在空气中要变质,KOH 也有类似的化学性质。某研究性学习小组发现一瓶未密封的 KOH 固体,对其成分提出以下假设,并完成了实验探究。
假设一:只含 KOH;
假设二:___________;
假设三:只含 K2CO3 。
Ⅰ.成分中可能含有 K2CO3的原因是_____________。
Ⅱ.进一步探究的过程如下:
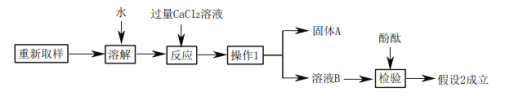
①操作1的名称是________。
②溶液 B 中含有的阳离子有______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】硫酸是重要的化工原料,可用于生产化肥农药火药等,硫酸生产厂产生的烟气中含有SO2气体,直接排放会形成酸雨,如图是某硫酸厂除去烟气中SO2的流程图,回答下列问题:
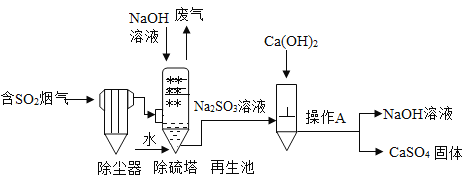
(1)除硫塔内,将NaOH溶液呈雾状向下喷洒,其目的是________;SO2发生反应的化学方程式是________(写一个)。
(2)再生池内加入的氢氧化钙也可用________代替。
(3)图中操作A指的是________,流程中可以循环利用的物质是________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)“健康饮食、均衡营养”是青少年健康成长的重要保证。
①蛋白质是构成细胞的基本物质,是机体生长和修补受损组织的主要原料。处于生长发育期的青少年每天需要较多的蛋白质。下列物质中富含蛋白质的有_____(填字母)。

②“食品安全”是一个永恒的话题。你认为下列认识不科学的是_____(填字母)。
A 任何食品都不可以使用食品添加剂
B 霉变的大米、花生,即使经过蒸煮也不能食用
C 含钙、锌的奶粉有利于补充人体所需的常量和微量元素
D 用工业用盐亚硝酸钠代替食盐来腌渍食品
(2)“科技创新、材料发展”极大地促进了人类社会的进步。
①“辽宁号”航母的服役举世瞩目。钢铁是制造航母的主要材料,它易与空气中的水、_____等发生反应而锈蚀,请你列举一种防止钢铁锈蚀的方法_____。
②可降解塑料的问世,既方便了生活,又减少了“白色污染”。塑料属于_____材料(填“复合”或“合成”)。
(3)水是生命之源。请回答下列问题:
①硬水是指中含有较多_________(填微粒符号)的水。生活中,可用______________鉴别硬水和软水。
②如图为电解水的实验装置图,下列说法正确的是__________。
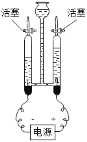
A在水中加入少量稀硫酸以增强水的导电性
B与正极相连的玻璃管内得到的气体能使带火星的木条复燃
C该实验中所得氢气和氧气的质量比约为 2:1
D根据该实验所得产物,说明水分子可分
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】电影《复仇者联盟》中,美国队长和蜘蛛侠使用的武器和衣服如图所示,请回答下列问题:

(1)图中标示的物质中,属于金属材料的是______________,属于有机合成材料的是___________。
(2)艾德曼合金钢属于____________(填纯净物或混合物),其含有主要元素是_____________(填元素符号),它与生铁的区别是________。
(3)科技的进步促进材料的发展,请你谈一谈化学材料与生活的关系_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室中常见装置,回答下列问题。
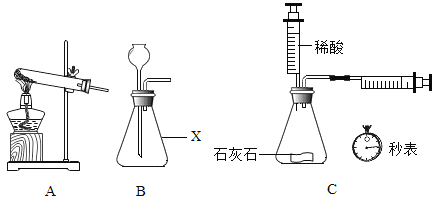
(1)仪器X的名称是______________。
(2)实验室用氯酸钾制取O2应选用的发生装置是______ ( 填字母序号)反应的化学方程式是______________,该反应属于______________(填反应类型)。
(3)利用图C装置探究不同地区石灰石与酸反应的剧烈程度。选用规格大小相同的不同地区的石灰石与等体积稀酸反应,从酸的角度说明还需要控制的变量有______________,实验时通过测定_____________来比较。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】过氧化镁(MgO2)是一种镁精细化工产品。在医疗上可用来治疗消化不良、胃酸过多等疾病。在环境保护方面,过氧化镁可用来处理地下水污染的土壤。还可以用于牙膏,对牙齿有漂白和防过敏的作用。某化学兴趣小组对过氧化镁的性质和制备等进行了以下研究。
一.过氧化镁的性质
(1)过氧化镁(其中氧元素的化合价为____)是一种白色的粉末,其外观与物理性质与氧化镁相似。化学性质不够稳定,不溶于水,但逐渐的被分解放出氧气。
过氧化镁有强氧化性,常温下比较稳定,但是加热时会分解生成氧气和氧化镁。请下出该反应的化学方程式________。
(2)过氧化镁易溶于稀盐酸,发生反应:MgO2+2HCl=MgCl2+H2O2同时温度升高,说明该反应热量__________(填“放出”或“吸收”)。
二.过氧化镁的制备
下图是利用碱式碳酸镁(Mg2(OH)2CO3)和30%的过氧化氢溶液来制取过氧化镁。
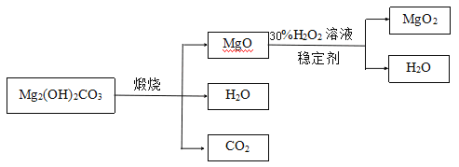
(资料)①碱式碳酸镁与碳酸镁有相似的化学性质,能与稀盐酸反应产生二氧化碳②氧化镁与过氧化氢反应放出大量的热
(3)检测煅烧过程碱式碳酸镁完全分解的方法是_________(写出具体的操作和现象);上述生产过程加入稳定的剂的作用是________。
(4)用上述碱式碳酸镁在550、600、650及700℃下煅烧一定的时间生成氧化镁。用上述条件制备的氧化镁分别与30%双氧水反应合成过氧化镁产率(见图1和图2)。
碱式碳酸镁煅烧的温度适宜控制在________℃,煅烧的时间适宜控制在______h。
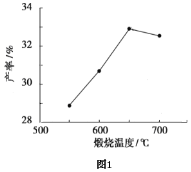
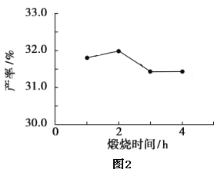
(5)结果在适宜的温度和时间下,碱式碳酸镁能完全分解,并且得到的氧化镁颗粒表面积最大,能与30%过氧化氢充分反应,所以产率高。推测700℃时,产率明显降低的可能的原因____。
三.过氧化镁产品纯度检测
在生产过程中,过氧化镁中常常含有少量的氧化镁杂质(其他杂质不考虑),以下是该小组进行纯度检测的实验装置和实验步骤。

①检查装置气密性,装入药品(样品质量为0.7g),调节刻度管使左右两边液面相平,刻度管度数为10.0mL。
②打开分液漏斗开关,待瓶中无气泡产生时,关闭开关。
③再次调节刻度管使左右两边液面相平,刻度管度数为122mL。
(6)稀盐酸中放入的少量硫酸铜溶液目的是__________。
(7)根据上面实验数据计算样品中过氧化镁的质量分数__________(写出具体的计算过程,实验条件下O2密度为1.429g/L)。
(8)该小组同学所测得质量分数比实际结果偏大,你觉得可能的原因是(_______)
A 生成的氧气有少量溶于水 B 未等装置冷却到室温就开始读数
C 杂质与盐酸反应能产生少量的气体 D 滴入的稀盐酸占了一部分气体的体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com