
【题目】根据空气的成分用物质的化学符号填空:
(1)小白鼠在装有空气的密闭容器中可存活一段时间,说明空气中含有 。
(2)石灰水长期露置在空气中会出现白色固体物质,说明空气中含有 。
(3)夏天,盛放冰棒的杯子外壁上附有一层水珠,说明空气中含有 。
科目:初中化学 来源: 题型:
【题目】下列关系图中,相连的两种物质间能发生化学反应。请回答有关的问题:

(1)若A是金属,C是FeSO4,则A是 (选填“Fe”“Cu”或“Mg”),写出反应②的化学方程式: ,该反应基本类型是 (选填“化合”、“分解”、“置换”或“复分解”)反应;图中物质B应该是 (填序号)。 A.Cu B.O2 C.NaOH D.Fe2O3
(2)若A是常用于改良酸性土壤的物质,B是非金属氧化物,C是一种蓝色的硫酸盐溶液,则A是 写出图中A和B反应的化学方程式: 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包含有碳酸钠和碳酸氢钠的混合物,为了测定其含量,小明取19g样品放入烧杯中,加入100g水充分溶解后,逐渐滴入稀盐酸并不断搅拌,至B点时恰好完全反应。测出烧杯中溶液总质量与加入稀盐酸质量的关系曲线如图所示(反应生成的气体全部逸出)。已知碳酸钠与稀盐酸反应分两步进行:
第一步反应:Na2CO3+HCl=NaCl+NaHCO3
第二步反应:NaHCO3+HCl=NaCl+H2O+CO2↑

回答下列问题:
(1)A点溶液的溶质为 (填化学式)
(2)图中AB段表示第 步反应;根据质量守恒定律,反应后生成的二氧化碳质量是 g。
(3)所加入的稀盐酸中溶质质量分数是多少?(写出计过程)(精确到0.1%)
(4)样品中碳酸氢钠的质量是 g。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】王安石的《梅花》诗:“墙角数枝梅,凌寒独自开.遥知不是雪,为有暗香来。”诗人在远处就能闻到淡淡的梅花香味的原因是( )
A.分子很小 B.分子在不断地运动
C.分子之间有间隙 D.分子是可以分的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】欲测定一瓶标签破损的稀硫酸的溶质质量分数。现取10g稀硫酸样品,将溶质质量分数为5%的氢氧化钠溶液逐滴加入到样品 中,进行了数字化实验,边加边搅拌,随着氢氧化钠溶液加入, 计算机描绘出了整个实验过程中溶液pH的变化图像(如图所示)。
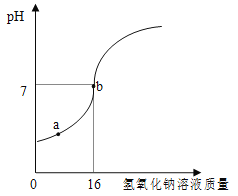
(1)b点溶液中溶质的化学式________。
(2)计算该稀硫酸的溶质质量分数。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】一包干燥的红色粉末可能由Cu、Fe2O3二种固体中的一种或两种组成。某化学兴趣小组对其组成进行探究。请你参与并回答下列问题。
[提出猜想]红色粉末可能的组成有:①只有Cu ②只有Fe2O3 ③Cu、Fe2O3的混和物。
[查阅资料]Cu在FeCl3中发生反应:2FeCl3+Cu=2FeCl2+CuCl2
[实验探究]

(1)甲同学取少量红色粉末于试管中,滴加足量稀盐酸,振荡后观察,发现固体全部溶解,甲同学认为可以排除猜想中的①和③,而乙同学认为只能排除猜想①,你认为的 观点正确(填“甲”或“乙”)。
(2)丙同学为进一步确定红色粉末的组成,称取该粉末5.0g,按如图所示装置在通风橱中进行实验,开始时缓缓通入CO气体,过一段时间后再加热使其充分反应,待反应完全后,停止加热,仍继续通CO气体直至试管冷却。反应前后称量相关装置和物质的总质量,其数据如下表。
反应前 | 反应后 | |
Ⅰ组 | 玻璃管和红色粉末的总质量为37.3g | 玻璃管和固体物质的总质量为36.1g |
Ⅱ组 | 洗气瓶和所盛溶液的总质量为180.0g | 洗气瓶和瓶中物质的总质量为183.1g |
[交流讨论]
(3)在装置A中先通入CO气体的作用是 。
(4)应该选择 组的实验数据进行计算来确定红色粉末的组成。最终计算结果表明,该红色粉末的组成是猜想中的第 组(填序号)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某研究人员按下图所示流程进行“燃煤烟气的脱硫研究”。实验中,SO2和O2混合气体连续通入,水和铁在起始时一次性加入,反应液多次循环。

(1)吸收池中发生反应的化学方程式是2SO2+2H2O+O2====2H2SO4,吸收时,温度不宜过高的原因是 。
(2)反应池中发生反应的化学方程式是 ;为确保反应液的循环吸收效果,反应池中的反应需控制在40℃左右进行,在此条件下欲加快该反应速率宜采取的措施有 。
(3)随着反应液流入吸收池中,吸收液中H2SO4的生成速率明显加快,其原因可能是 。
(4)经过多次循环后,反应液可以用来制备FeSO4·7H2O,它在医疗上常用于治疗 (选填字母)。
A.甲状腺肿大 | B.佝偻病 | C.龋齿 | D.贫血症 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com