
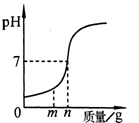
 在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示.
在用稀盐酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的酸碱度变化如图所示.分析 (1)氯化氢与氢氧化钠溶液反应生成氯化钠和水,据此写出反应的化学方程式;
(2)根据坐标变化的趋势结合盐酸的pH小于7,氢氧化钠溶液的pH大于7分析;
(3)当加入溶液的质量为ag时,溶液呈现酸性,溶液中既有生成的氯化钠,又有未反应的盐酸.
解答 解:(1)稀盐酸与氢氧化钠溶液反应生成氯化钠和水,反应的化学方程式为:HCl+NaOH=NaCl+H2O,
故答案为:HCl+NaOH=NaCl+H2O;
(2)坐标的pH变化是由小于7到大于7的过渡,因此进行的操作是将氢氧化钠溶液滴加到稀盐酸中,
(3)当加入溶液的质量为ag时,溶液呈现酸性,所得溶液中的溶质为氯化氢和氯化钠,
故答案为:HCl、NaCl.
答案:
(1)HCl+NaOH=NaCl+H2O;
(2)氢氧化钠溶液;稀盐酸;
(3)HCl、NaCl.
点评 本题考查了酸碱混合的定性判断、化学方程式的书写,题目难度中等,解答本题的关键是根据坐标的pH变化结合溶液的酸碱性与溶液pH的关系进行分析,并对反应过程中的溶液的酸碱性正确判断.


 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:多选题

| A. | 铱原子的相对原子质量为192.2g | B. | 铱原子的核外电子数为77 | ||
| C. | 铱属于非金属元素 | D. | 铱元素符号为Ir |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
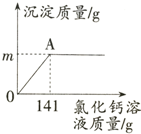 某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:
某纯碱样品中含有少量氯化钠,取该样品11g,全部溶液在100g水中,再逐渐滴加氯化钙溶液,反应的情况如图所示,A点时,过滤,得到滤液242g,计算:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 下图是同学们经常使用的铅笔,在组成铅笔的各种材料中.
下图是同学们经常使用的铅笔,在组成铅笔的各种材料中.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com