
【题目】硬水受热后会产生水垢,水垢的主要成分是CaCO3和Mg(OH)2,其它成分不参与反应.实验室由水垢制取纯净CaCl2固体的流程如下:
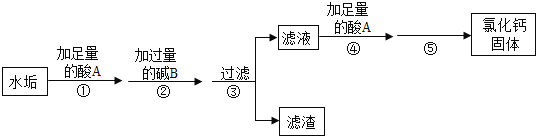
请按要求填空:
(1)酸A是人体胃酸的主要成分,酸A的化学式是_____;
(2)步骤②中生成沉淀的化学反应方程式是______;
(3)步骤③中用到的玻璃仪器主要有烧杯、漏斗、______、其作用是_________
(4)步骤④加酸A的作用是______;
(5)步骤⑤是利用______的方法得到氯化钙固体.
 阳光课堂同步练习系列答案
阳光课堂同步练习系列答案科目:初中化学 来源: 题型:
【题目】化学方程式书写正确且属于复分解反应的是
A. NaOH+H2SO4→NaSO4+H2O
B. Fe+H2SO4→FeSO4+H2↑
C. 2NaOH+CuSO4→Na2SO4+Cu(OH)2↓
D. 2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验室有100g废液,其中含有硫酸铜、硫酸亚铁、硫酸锌。现对废液进行处理,得到铜和硫酸锌溶液,实验流程如下图所示。
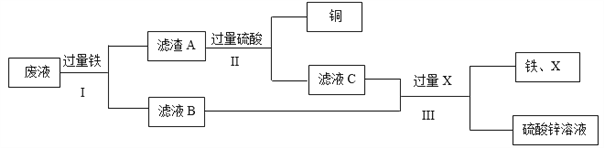
①步骤I、II、III中均包含的操作名称是_____。
②滤液B中的溶质是___________________。
③当观察到________时,说明滤渣A中铁已经完全反应。
④步骤III中加入的X是_________。
⑤实验结束后,生成0.1mol铜,请计算原废液中硫酸铜的溶质质量分数。
(根据化学方程式列式计算)___________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】【2016年湖南省永州市】铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为( )
A.24 B.58 C.82 D.140
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】【2016年湖北省鄂州市】下列化学用语与意义相符的是
A.N2:表示2个氮原子
B.Fe3O4:表示该物质中铁元素与氧元素的质量比为3:4
C.S2-:表示硫元素显-2价
D.C2H5OH:表示该物质由三种元素组成,且1个分子中含9个原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质组成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。
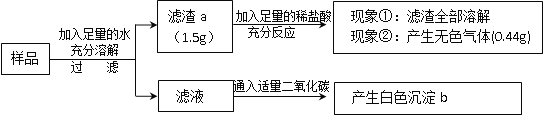
下列说法不正确的是
A. 滤渣a的成分是碳酸钙和氢氧化镁
B. 滤液中溶质的成分除氯化钠还有氢氧化钠、硫酸钠
C. 白色沉淀b的成份是碳酸钡
D. 若现象①“滤渣全部溶解”变为“滤渣部分溶解”,其他现象不变,则不能确定原样品中一定存在氯化镁
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】【2015年浙江省台州市】下列有关化学符号“H2O”表示的意义,正确的是( )
A.水这种物质 B.水由氢原子和氧原子构成
C.一个水分子中含有一个氢分子 D.水由两个氢元素和一个氧元素组成
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】镁条在空气中久置表面会变黑。某小组同学设计并进行实验,探究镁条变黑的条件。
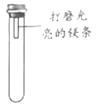
【查阅资料】常温下,亚硫酸钠(Na2SO3)可与O2发生化合反应。
【猜想与假设】常温下,镁条变黑可能与O2、CO2、水蒸气有关。
【进行实验】通过控制与镁条接触的物质,利用右图装置(镁条长度为3cm,试管容积为20mL),分别进行下列5个实验,并持续观察20天。
编号 | 主要实验操作 | 实验现象 |
1 | 先充满用NaOH浓溶液洗涤过的空气 再加入2mL浓硫酸 | 镁条始终无明显变化 |
2 | 加入2mL NaOH浓溶液 | 镁条始终无明显变化 |
3 | 先加入2mL浓硫酸 再通入约4mL CO2 | 镁条始终无明显变化 |
4 | 先加入4mL饱和Na2SO3溶液 再充满CO2 | 镁条始终无明显变化 |
5 | 先加入2mL蒸馏水 再通入约4mL CO2 | 镁条第3天开始变黑 至第20天全部变黑 |
【解释与结论】
(1)实验1和2中,NaOH浓溶液的作用是____________(用化学方程式表示)。
(2)实验1的目的是____________。
(3)实验3中,试管内的气体主要含有CO2、__________。
(4)得出“镁条变黑一定与CO2有关”结论,依据的两个实验是___________(填编号)。
(5)由上述实验可推知,镁条变黑的条件是___________。
【反思与评价】
(6)在猜想与假设时,同学们认为镁条变黑与N2无关,其理由是__________。
(7)欲进一步证明镁条表面的黑色物质中含有碳酸盐,所需要的试剂是__________。
【定量分析】小陆同学取了实验室存放较久的1克镁条和20克稀硫酸(足量)放入一支质量为30克的试管中,看到产生较多气泡,等没有气泡后精确称量,得到试管和内容物总质量为50.92克,小陆同学认为此反应产生的全部为氢气。试帮小陆同学计算这1 克镁条中还含有多少镁?
__________
同学们经过讨论一致认为在操作和称量准确的情况下,实际含有的镁要小于计算结果。请你分析可以有原因_____________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com