

分析 (1)根据甲装置是碳酸钙在高温的条件下生成氧化钙和二氧化碳,二氧化碳进入戊中参与反应,丙中发生的反应是氧化钙和水反应生成氢氧化钙进行分析;
(2)根据质量守恒定律进行分析;
(3)根据设备丁中的反应是氢氧化钙和氯化铵反应生成氯化钙、氨气和水进行分析.
解答 解:(1)甲装置是碳酸钙在高温的条件下生成氧化钙和二氧化碳,二氧化碳进入戊中参与反应,丙中发生的反应是氧化钙和水反应生成氢氧化钙,化学方程式为:CaO+H2O═Ca(OH)2;
(2)化学反应前后元素种类不变,设备乙中的生成物是碳酸氢钠和氯化铵,所以反应物所含元素除C、H、O外,还有Na、N、Cl;
(3)设备丁中的反应是氢氧化钙和氯化铵反应生成氯化钙、氨气和水,所以设备丁中反应后的产物是CaCl2、NH3、H2O.
故答案为:(1)CaO+H2O═Ca(OH)2;
(2)Na、N、Cl;
(3)CaCl2、NH3、H2O.
点评 在解此类题时,首先分析题中考查的问题,然后结合学过的知识和题中的提示进行解答.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:初中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ①②③ | C. | ④⑤ | D. | ①②③⑤ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
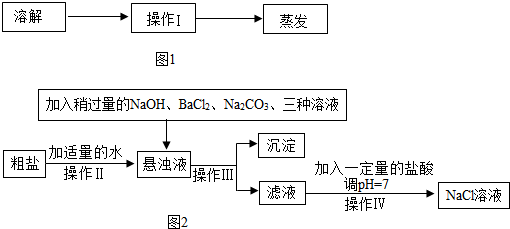
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(括号内为杂质) | 试剂 | 操作方法 |
| A | CO2气体(CO) | 过量的氧气 | 点燃 |
| B | Fe2O3(Fe) | 足量的盐酸 | 过滤 |
| C | FeSO4溶液(CuSO4) | 足量的锌 | 过滤 |
| D | O2(H2O) | 浓硫酸 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
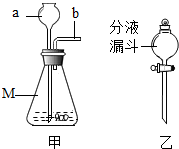 如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )
如图中的甲装置可作为实验室制二氧化碳的发生装置,下列说法正确的是( )| A. | M所指仪器的名称是广口瓶 | |
| B. | 仪器a、b插入双孔橡皮塞的先后顺序是先a后b | |
| C. | 甲装置也可以用作实验室制氧气和氢气的发生装置 | |
| D. | 将甲中a换成仪器乙,优点是能控制反应的发生与停止 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在雾霾治理过程中,可注重空气中氨气的检测及控制氨气的排放 | |
| B. | PM2.5专用口罩中使用了活性炭,是利用了活性炭的吸附性 | |
| C. | 为有效控制雾霾,应禁止使用氮肥 | |
| D. | 该反应原理中所有元素化合价都不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | A的溶解度比B大 | B. | B的溶解度比A大 | ||
| C. | 二者的溶解度相等 | D. | 无法比较二者的溶解度大小 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
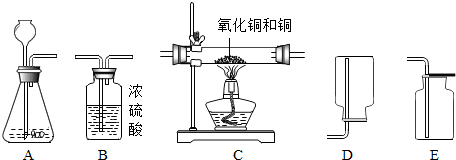
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com