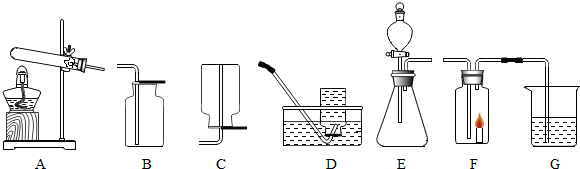
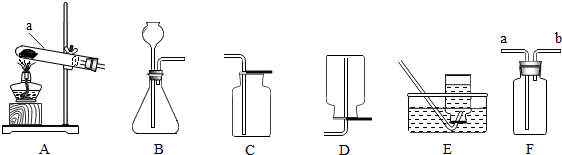
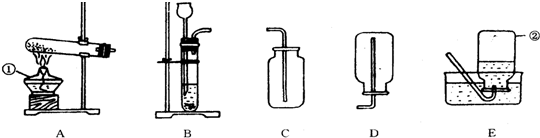
解:(1)实验室常用稀盐酸和石灰石制取二氧化碳,石灰石的主要成分是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,方程式是:CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;该反应不需加热,属于固液常温型,故选发生装置B;可用燃着的木条放于瓶口观察是否熄灭进行验满;
(2)加热氯酸钾和二氧化锰混合物的方法制取氧气,同时生成氯化钾和氧气,方程式是:2KClO
3
2KCl+3O
2↑;金属锌和稀硫酸反应制取氢气,同时生成硫酸锌,方程式是:Zn+H
2SO
4(稀)=ZnSO
4+H
2↑;氢气的密度比空气小且难溶于水,故可用向下排空气法或排水法收集;
故答案为:
(1)CaCO
3+2HCl=CaCl
2+H
2O+CO
2↑;B;用燃着的木条放在集气瓶口,观察木条是否熄灭
(2)2KClO
3
2KCl+3O
2↑;Zn+H
2SO
4=ZnSO
4+H
2↑;C(或E)
分析:根据实验室制取二氧化碳、氧气、氢气的反应原理书写方程式,依据反应物的状态选择发生装置,依据气体的密度和溶解性确定收集装置,并依据二氧化碳不能支持燃烧用燃着的木条放于瓶口观察是否熄灭进行验满.
点评:掌握实验室制取二氧化碳、氧气和氢气的方法,发生和收集装置的选取方法才能正确解答.

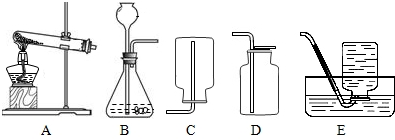
 2KCl+3O2↑;金属锌和稀硫酸反应制取氢气,同时生成硫酸锌,方程式是:Zn+H2SO4(稀)=ZnSO4+H2↑;氢气的密度比空气小且难溶于水,故可用向下排空气法或排水法收集;
2KCl+3O2↑;金属锌和稀硫酸反应制取氢气,同时生成硫酸锌,方程式是:Zn+H2SO4(稀)=ZnSO4+H2↑;氢气的密度比空气小且难溶于水,故可用向下排空气法或排水法收集; 2KCl+3O2↑;Zn+H2SO4=ZnSO4+H2↑;C(或E)
2KCl+3O2↑;Zn+H2SO4=ZnSO4+H2↑;C(或E)

 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案 黄冈创优卷系列答案
黄冈创优卷系列答案
 收集装置是
收集装置是