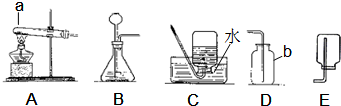
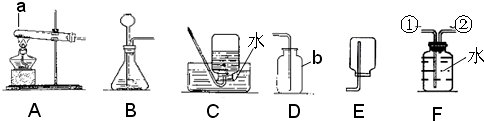
解:(1)依据常用仪器可知,a、b 分别是试管和集气瓶;
故答案为:试管、集气瓶;
(2)实验室制取二氧化碳用大理石与稀盐酸反应生成二氧化碳、氯化钙和水;该反应属于固体和液体混合且不需加热,所以选择发生装置B,另外二氧化碳的密度比空气大且能溶于水,所以只能用向上排空气法收集;
故答案为:CaCO
3+2HCl═H
2O+CaCl
2+CO
2↑; B; D;
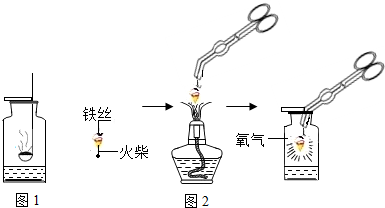
(3)高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气;该反应属于加热固体的反应,所以选择发生装置A;氧气的密度比水小,所以应从短管进入;
故答案为:2KMnO
4
K
2MnO
4+MnO
2+O
2↑; A; ②;
(4)实验室用加热无水醋酸钠和碱石灰的固体混合物的方法制取甲烷,所以选择发生装置A;甲烷是一种难溶于水的气体,且其密度比空气小,所以可用排水法或向下排空气法收集;
故答案为:A、C(或AE、AF);
(5)依据质量守恒定律,生成氧气的质量是:15.5克-10.7克=4.8克;
设生成氯化钾的质量是X
2KClO
3
2KCl+3O
2↑
149 96
X 4.8克
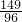
=
X=7.45克
答:生成氧气4.8克,同时生成氯化钾7.45克.
分析:(1)根据常用仪器回答;
(2)根据实验室制取二氧化碳的反应原理书写方程式;并依据装置的选取方法判断发生和收集装置;
(3)根据高锰酸钾制取氧气的反应原理书写方程式;依据反应物和反应条件选择发生装置;氧气的密度比水小,所以应从短管进入;
(4)根据题意和装置的选取方法选择相应的装置组合;
(5)依据质量守恒定律,生成氧气的质量是反应前后固体质量的差;然后根据氧气的质量和方程式求氯化钾的质量.
点评:本题考查了实验室制取氧气和二氧化碳的装置选取、方程式的书写、方程式计算等知识,很好的考查了学生对知识的掌握和应用.

 K2MnO4+MnO2+O2↑; A; ②;
K2MnO4+MnO2+O2↑; A; ②; 2KCl+3O2↑
2KCl+3O2↑ =
=