
【题目】金属元素钼(Mo)通常用作合金及不锈钢的添加剂。如图是化工生产中制备金属钼的主要流程图。
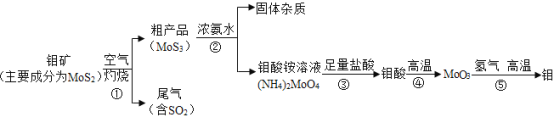
(1)步骤①中,灼烧钼矿通常会将矿石粉碎成小颗粒,其目的是_______________。
(2)如果在实验室模拟步骤②,需要使用的主要玻璃仪器有_____(填字母序号)。
A烧杯 B玻璃棒 C漏斗 D酒精灯
(3)流程图中的物质属于氧化物的有_________________________________________。
科目:初中化学 来源: 题型:
【题目】某兴趣小组在制取氧气的实验过程中,有如下实验设计方案,该方案的实验目的是:探究氯酸钾和二氧化锰的质量比对反应速率的影响。
编号 | 温度 | 催化剂 | 氯酸钾、二氧化锰的质量比 | 生成1升氧气所需时间/s |
实验Ⅰ | 400℃ | MnO2 | 1:1 | 153 |
实验Ⅱ | 400℃ | MnO2 | 2:1 | 240 |
小芳在实验时,误把氧化铜当作二氧化锰放入加热,结果发现也能较快产生氧气,于是进行如下探究:
猜想Ⅰ:除二氧化锰、氧化铜外,氧化铁(Fe2O3)也可以作氯酸钾分解的催化剂。
(设计实验)按下表进行实验,并测定开始产生气体时的温度(提示:开始产生气体的温度越低,表示反应速度越快)。
实验编号 | 实验药品 | 分解温度(℃) |
① | 氯酸钾 | 580 |
② | 氯酸钾和二氧化锰(质量比1︰1) | 350 |
③ | 氯酸钾和氧化铜(质量比1︰1) | 370 |
④ | 氯酸钾和氧化铁(质量比1︰1) | 390 |
(数据和结论)
(1)由实验_______与实验④对比,证明猜想合理;
(2)实验所用的三种物质中,催化效果最好的是_______。
(反思)
若要证明氧化铁是该反应的催化剂,还需验证它在化学反应前后的________和_______是否改变。
猜想Ⅱ:过氧化钙与水反应可制取氧气。
实验装置 | 实验主要过程 |
| ①检查装置气密性。 ②加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体。该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出。 |
实验结论:过氧化钙与水反应可制取氧气。
(分析与反思)
同学们对过氧化钙与水反应的生成物猜想如下:①氢氧化钙和氧气②碳酸钙和氧气
你认为猜想______(填序号)一定是错误的,理由是________,过氧化钙与水反应虽然没有快速收集到大量氧气,但过氧化钙在水中持续、缓慢放出氧气,因此小林认为渔民用过氧化钙做增氧剂。写出此反应的符号表达式________。
(计算)
该兴趣小组的同学们购得用于增氧的过氧化钙产品(杂质不含钙元素),标签如图所示。试计算:

(1)过氧化钙的相对分子质量为_______
(2)该产品中过氧化钙的质量分数至少为______。
(3)小组同学将3g某物质在制得的足量氧气中充分燃烧生成4.4g二氧化碳和1.8g水,求该物质中各元素的原子个数比(写出计算过程)。______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图所示装置可用于测定空气中氧气的含量,实验前在集气瓶内加入少量水,并做上记号。下列说法中不正确的是
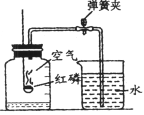
A. 该实验证明空气中氧气的体积含量约占1/5
B. 实验时红磷一定要过量
C. 实验前一定要检验装置的气密性
D. 红磷燃烧产生大量的白烟,火焰熄灭后立刻打开弹簧夹
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下面是几种实验室制取气体的发生与收集装置。
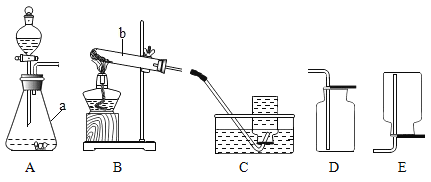
①写出图中的仪器名称:a _______ b_______
②写出用A为发生装置制取氧气的化学方程式:____________,该反应的基本类型是______。
③用D装置收集氧气时,验满方法是 _______ 。
④实验室用B装置取氧气并用C装置收集氧气,有关实验操作有:
a 加热;b 检查装置气密性;c 向试管中装入药品;d 当有连续气泡时用排水法收集; e 实验完毕将导气管从水槽中取出;f 熄灭酒精灯;g 将试管固定在铁架台上
正确顺序是_________。(填序号)
下图是取用该实验的相应药品操作,其中正确的是_______ (选填编号)。
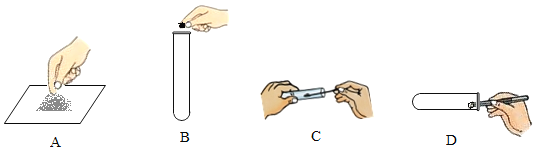
实验结束后,收集到的氧气不纯,其原因是:_________ (写一点)。
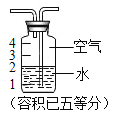
⑤用如图装置排水收集氧气后,集气瓶中氧气的体积分数是_______(列式即可)。
⑥下图是探究木炭在纯氧中燃烧的实验操作:
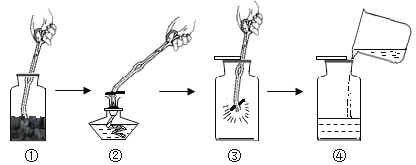
请推断:操作流程d中用烧杯倾倒的液体是______,现象是________,得出的探究结论是_______。
⑦现有0.2mol氯酸钾和一定量的二氧化锰完全反应,能制得氧气的物质的量为多少______?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】 一氧化碳,分子式CO,是无色、无味气体,剧毒。比空气略轻。在水中的溶解度很小。一氧化碳是含碳物质不完全燃烧的产物。也可以作为燃料使用。煤和水在高温下可以生成水煤气(一氧化碳与氢气的混合物)。有些现代技术,如炼铁,会产生副产品一氧化碳。它为中性气体。燃烧时发出蓝色的火焰,放出大量的热。因此一氧化碳可以作为气体燃料。一氧化碳作为还原剂,高温或加热时能将许多金属氧化物还原成金属单质,因此常用于金属的冶炼。由于一氧化碳与体内血红蛋白的亲和力比氧与血红蛋白的亲和力大200-300倍,而碳氧血红蛋白较氧合血红蛋白的解离速度慢3600倍,当一氧化碳浓度在空气中达到35ppm,就会对人体产生损害,会造成一氧化碳中毒。工业上炼钢、炼焦、烧窑等在生产过程中炉门或窑门关闭不严,煤气管道漏气,汽车排出尾气,都可逸出大量的一氧化碳。北方冬季用煤炉、火炕取暖因燃烧不完全而产生一氧化碳。一氧化碳中毒的症状有头晕、头痛、恶心、呕吐、反应迟钝,严重时出现深昏迷。当发现或怀疑有人为一氧化碳中毒时,应立即采取下述措施:立即打开门窗通风;确保呼吸道通畅;迅速送往有高压氧治疗条件的医院。
(1)一氧化碳的物理性质为___________________。
(2)为了预防煤气中毒,冬季用煤炉取暖的家庭下列措施正确的是_______。
a在煤炉或床头放一盆冷水 b烟道连接处用胶条密封
(3)CO中毒的原理是一氧化碳与体内血红蛋白的亲和力比氧与血红蛋白的亲和力______倍。
(4)工业用煤和水生产水煤气的化学方程式是__________________。
(5)CO用于工业炼铁,写出此反应的化学方程式________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图像不能正确反映对应变化关系的是
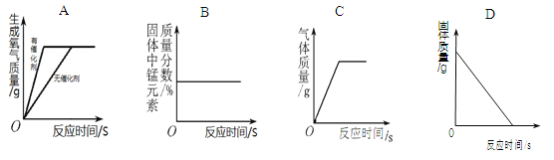
A. 用相同的过氧化氢溶液分别制取氧气
B. 加热一定量的高锰酸钾固体
C. 加热一定量的氯酸钾和二氧化锰的混合物
D. 硫粉在足量的氧气中充分燃烧
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用w型玻璃管进行如下微型实验:先对a处物质加热使之燃烧,然后将注射器中的过氧化氢溶液推入管中与二氧化锰接触,并始终控制液体不进入a处。下列说法正确的是( )
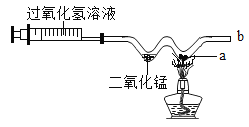
A. 若a处粉末是木炭粉,实验过程中能看到木炭燃烧,冒白烟
B. 该实验证明二氧化锰是过氧化氢溶液分解的催化剂
C. 推入过氧化氢溶液后,要对准二氧化锰处加热才能产生氧气
D. 本实验可以得出氧气浓度越大,燃烧越剧烈的结论
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图象能正确反映对应变化关系的是的质量( )
A.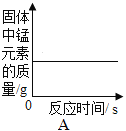 用酒精灯加热一定质量的高锰酸钾固体
用酒精灯加热一定质量的高锰酸钾固体
B.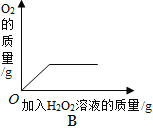 向盛有少量二氧化锰的烧杯中不断加入过氧化氢溶液
向盛有少量二氧化锰的烧杯中不断加入过氧化氢溶液
C.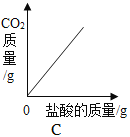 一定质量的石灰石中不断加入盐酸
一定质量的石灰石中不断加入盐酸
D.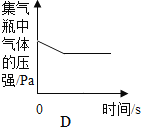 利用红磷燃烧测定空气中氧气的含量(打开止水夹前)
利用红磷燃烧测定空气中氧气的含量(打开止水夹前)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某同学自己设计的装置:用大塑料瓶子截去瓶底,留瓶口一段约8cm~10cm,瓶口配一胶塞由里往外塞紧。A、B两极是用镀铬曲别针伸直做成,由塞子露头处连接导线。试回答:
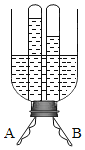
(1)其所用电源为______电,由图可知A端为______极。
(2)与A端相连的试管中得到的气体是_______,检验的方法是_____________。
(3)若与B端相连试管中气体的体积为8mL,则与A端相连试管中气体的体积为______。
(4)在某次电解水的实验中加入了少量的氢氧化钠(NaOH)溶液,目的是________________。 测得了分别与电源正负两极相连的阳、阴两极上产生的气体的实验数据如下:
时间/分钟 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
阴极生成气体体积(cm3) | 6 | 12 | 20 | 29 | 39 | 49 | 55 | 65 | 75 | 85 |
阳极生成气体体积(cm3) | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
仔细分析以上实验数据,1~6分钟内阴、阳两极产生气体的体积之比大于2:l,可能的原因是__________________。
(5)如图为水电解过程的微观示意图,你能从图中能得出哪些信息(写出三条)。

①物质组成方面__________________________;
②变化类型方面__________________________;
③微观变化方面__________________________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com