
【题目】化学概念通常呈现以下三种关系。下表中有关关系的建构正确的是
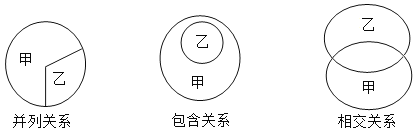
选项 | 甲 | 乙 | 甲乙之间关系 |
A | 有机物 | 无机物 | 包含关系 |
B | 分子 | 原子 | 相交关系 |
C | 化合反应 | 氧化反应 | 并列关系 |
D | 营养素 | 蛋白质 | 包含关系 |
A.AB.BC.CD.D
科目:初中化学 来源: 题型:
【题目】海水晒盐可制得粗盐,粗盐除氯化钠外,还含有 MgCl2、CaCl2、Na2SO4 以及泥沙等杂质,以下是某化学兴趣小组制定的一套制备精盐的实验方案,步骤如图所示:

(查阅资料)
可溶性钡盐有剧毒,可以导致蛋白质变性,破坏体内各种酶,使一系列生理活动被破坏。
(交流与表达)
(1)步骤①中玻璃棒的作用是__________,溶解粗盐时所加水的质量不宜过多,也不宜 过少,过多会造成__________,过少会使得精盐的产率__________(填“偏高”或“偏 低”)。
(2)下列试剂 X 符合要求的是__________(选填字母)。
A氧化钙 B氢氧化钡溶液 C氢氧化钠溶液 D氢氧化钙溶液 E氢氧化钾溶液
(3)氯化钡溶液和碳酸钠溶液的添加顺序__________(填“能”或“不能”)颠倒,沉淀 B 中的成分是 BaSO4、CaCO3 和(填化学式)_________,加入盐酸的作用是__________。
(4)某同学为了证明溶液 C 是否有盐酸剩余,设计的下列方法中正确的是_________(选填字母)。
A取样,加入铜,若无现象,说明盐酸没有剩余
B取样,测溶液 pH,若 pH<7,说明盐酸有剩余
C取样,加碳酸钠溶液,若有气泡产生,说明有盐酸剩余
D取样,加硝酸银溶液,若有白色沉淀产生,说明有盐酸剩
(反思与评价)
(5)小刚同学认为该方案实际得到的氯化钠比原粗盐中含有的氯化钠要多,请你为他找出理由_________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】室温下,将盛有接近饱和的硝酸钾溶液的小烧杯放在盛水的大烧杯中,如图所示,欲使硝酸钾溶液变为饱和溶液,可向大烧杯中加入的固体物质是
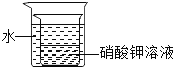
A.氧化钙B.氯化钠C.硝酸铵D.氢氧化钠
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是实验室制取和收集气体常用装置。根据要求回答下列问题。
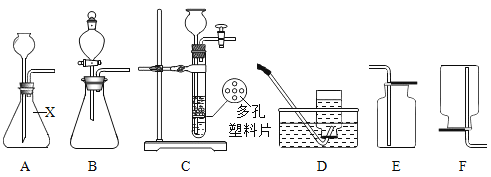
(1)仪器X的名称为__________________。
(2)若用碳酸钠粉末和稀盐酸制取少量CO2,宜采用的发生装置和收集装置组合是__________________。(填字母序号)
(3)若用上述适宜的发生装置制取氧气,则反应的化学方程式为__________________。若要收集氧气做铁丝燃烧的实验,最适宜的收集装置是__________________。 (填字母序号)
(4)若用锌粒和稀硫酸反应制取氢气,并选择装置C作发生装置,相比较C装置的优点是____。氢气作为新能源有许多优点,但是大量使用氢气还有一定的困难,原因是_____________(写一点即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】老师在分析金属和盐溶液反应时指出在金属活动性的顺序里,位于前面的金属能把排在后面的金属从它们的盐溶液中置换出来,但钾、钙、钠除外。李明同学很好奇,于是做了钠与硫酸铜溶液反应的实验。
(进行试验)
一块4.6g的金属钠,放入盛有一定量硫酸铜溶液的烧杯中,发现金属钠浮在液面上不停打转,产生大量气体,烧杯发烫,溶液中出现了蓝色絮状沉淀,并没有出现紫红色的铜,一会儿,部分沉淀逐渐变黑。充分反应后,冷却过滤,得到滤液是无色。
(提出问题)
金属钠与硫酸铜溶液反应后的产物是什么?无色滤液的成分是什么?
(查阅资料)
(1)①钠能与水反应生成一种碱,同时放出气体。
②氢氧化铜受热至60℃ ~80℃变暗,温度过高时分解为相应的金属氧化物和水。
(实验探究1)探究生成的气体是什么?
李明同学将上述实验药品放入锥形瓶中,立即塞上带导管的单孔塞,将导管通入肥皂水中,将燃着的木条靠近飘起的肥皂泡,有爆鸣声。说明生成的气体是____________。
(实验探究2)探究沉淀的成分是什么?
(猜想与假设)沉淀中有Cu(OH)2和CuO,还可能含有Cu。
(实验验证)
实验步骤 | 实验现象 | 结论 |
将锥形瓶内反应后过滤所得滤渣放入烧杯内,并加入足量的______ | _________ | 沉淀中没有Cu |
(实验结论)
通过实验,李明同学得出结论:钠加入硫酸铜溶液会先与水反应,生成的碱再与硫酸铜反应生成氢氧化铜。写出生成的碱与硫酸铜反应的化学方程式______________。
(实验探究3)滤液的成分是什么?
通过分析,李明同学得出:所得的无色滤液中一定含有硫酸钠,还可能含有______________。
若要证明是否含有该物质,只需向无色滤液中滴加______________ (填物质名称)观察现象即可获得结论。
(反思与交流)
(1)出现黑色物质的可能原因是______________。
(2)设计一个简单实验证明硫酸铜溶液显蓝色是由Cu2+引起的。你的方案是______________。(要求写出实验步骤和现象)
(3)钠完全反成后,所得无色滤液中硫酸钠的质量若用a表示,则a的取值范围是______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭,导弹,航天飞机船舶等,下图为某化工企业生成钛流程示意图:
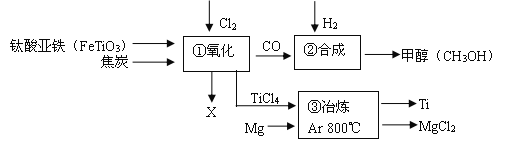
请回答下列问题:
(1)FeTiO3中钛元素的化合价为: ;
(2) ①中化学方程式为2FeTiO3+6C +7Cl2 ![]() 2X +2TiCl4 +6CO,则 X为
2X +2TiCl4 +6CO,则 X为
(填化学式)。
(3)②中CO和H2以化学计量数1:2恰好完全反应,则该反应的基本反应类型是 。
(4)③中氩气的作用是 ,
该步反应的化学方程式为 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】A﹣K为中学常见的物质,其中A为黑色粉末,H是一种建筑材料的主要成分,它们之间的转换关系如图所示:

(1)D,F的化学式:D ,F 。
(2)①的基本反应类型是 。
(3)反应②的化学方程式是 。
(4)气体E的用途是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】纯碱(Na2CO3)是一种重要的有机化工原料。侯氏制碱法制出的纯碱常含少量NaCl杂质,化学兴趣小组对工业纯碱样品进行实验探究。
Ⅰ研究Na2CO3的性质
(1)Na2CO3溶液显____(填“酸性”、“中性”或“碱性”)。
(2)检验样品中碳酸根的方法是____。
Ⅱ设计以下实验方案,测定样品中Na2CO3的质量分数。
[方案一]取一定质量样品,置于小烧杯中,加适量水溶解;向小烧杯中加入足量Ba(OH)2溶液,过滤,洗涤、干燥沉淀,称量固体质量,计算。
(3)过滤操作中,除了烧杯、漏斗外,还要用到的玻璃仪器为____。
(4)实验中判断沉淀是否完全的方法是____。
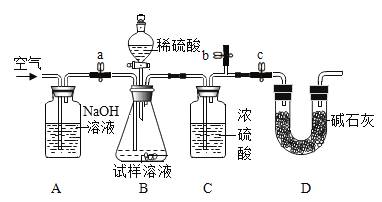
[方案二]采用如图装置,检查装置气密性;称取样品m1g于锥形瓶中,称装置D质量为m2 g;关闭止水夹c,打开止水夹a、b,缓慢鼓入空气数分钟,关闭止水夹a、b,打开止水夹c,缓慢加入稀硫酸至不再产生气体为止;打开止水夹a,缓慢鼓入空气数分钟,再称量装置D质量为m3g。
(查阅资料)浓硫酸具有吸水性,碱石灰的成分为CaO和NaOH固体
(5)装置B中发生的化学方程式为______。
(6)样品中Na2CO3的质量分数的计算式是______。
(7)反应后鼓入空气的目的是______。
(8)该测定结果比实际值偏高,从装置上分析其原因可能是______;改进措施为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列是四种实验操作中各量变化关系的图像,能正确反映其对应操作的图像有
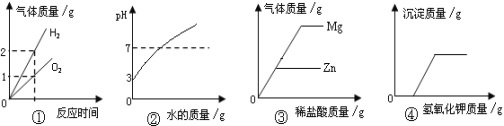
①电解水
②向一定量pH=3的盐酸溶液中不断加水稀释
③向等质量的镁和锌中分别加入溶质质量分数相同的稀盐酸至过量
④向盐酸和氯化铜的混合溶液中不断滴加氢氧化钾溶液
A.4个 B.3个 C.2个 D.1个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com