
科目: 来源: 题型:
【题目】下列各组物质间能通过一步反应就能实现如图转化的是( )
X | Y | Z | |
A | Fe | FeCl2 | Fe2O3 |
B | O2 | CuO | Cu |
C | AgNO3 | Ba(NO3)2 | BaSO4 |
D | Ca(OH)2 | NaOH | H2O |

A. AB. BC. CD. D
查看答案和解析>>
科目: 来源: 题型:
【题目】三角烯(化学式为C22H14)应用于量子计算、量子信息处理和自旋电子学等领域。下列说法中正确的是( )
A. 三角烯属于有机高分子化合物
B. 三角烯中含有氢分子
C. 三角烯中碳、氢元素的质量比为11:7
D. 三角烯中碳元素的质量分数大于90%
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们从山上采集到一种石灰石样品,为了测定石灰石样品中碳酸钙的质量分数(石灰石中的杂质不与盐酸反应,也不溶于水),取45g石灰石样品,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示,请计算:

(1)45g这种石灰石样品中碳酸钙的质量是_____g
(2)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
(3)列式计算45g石灰石与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数?_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学学习小组的同学在学习了《常见的酸》以后,对蚊虫分泌的让人痛痒不止的蚁酸产生了兴趣。他们在老师指导下对蚁酸进行探究。
(查阅资料)蚁酸的主要成分是甲酸,甲酸的化学式为HCOOH;甲酸溶于水,在一定条件下发生分解反应生成两种氧化物。
(提出问题)甲酸溶液是否具有酸性?
(实验与结论)向盛有甲酸溶液的试管中滴加紫色石蕊溶液,观察到溶液颜色变成红色,说明甲酸溶液显____性。
(提出问题)甲酸分解生成的两种氧化物是什么?
(推断与猜想)
⑴小组同学根据甲酸中含有氢元素,推测出生成物中含有水。
⑵他们对另一种氧化物提出两种猜想:猜想①:二氧化碳;猜想②:一氧化碳。
(实验与结论)
为了证明自己的猜想,他们将甲酸分解产生的气体通过如下图所示的装置(铁架台已略去)。
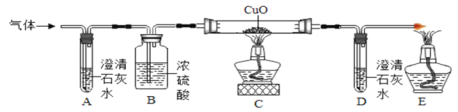
观察到的实验现象如下:
Ⅰ.装置A中澄清石灰水无明显变化。
Ⅱ.装置C中的黑色粉末变红色。
Ⅲ. 装置D中澄清石灰水变浑浊。
(实验结论)甲酸具有酸性,在一定条件下分解生成水和_______。
(拓展延伸)人被蚊虫叮咬后,在其叮咬处涂抹______________可减轻痛痒。
查看答案和解析>>
科目: 来源: 题型:
【题目】人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.
(1)西汉时期中国古老的冶铜方法是“湿法冶铜”主要的反应原理是铁与硫酸铜溶液反应,写出反应的化学方程式_____.
(2)铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图.
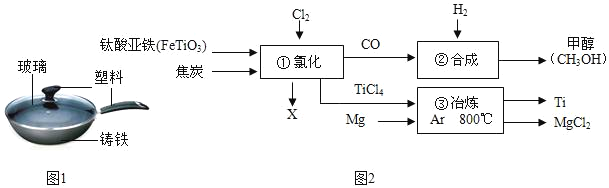
①铁锅含有的有机合成材料是_____.(填写名称).
②炒菜时铁锅中的油着火可用锅盖盖灭,其原理是_____.
③铜也易生锈,铜锈的主要成分是碱式碳酸铜(Cu(OH)2CO3),是铜与空气中的氧气、水和_____共同作用的结果.
(3)钛和钛合金被认为是21世纪的重要金属材料,被广泛用于火箭、导弹、航天飞机、船舶等,如图为某化工企业生产钛流程示意图:
请回答下列问题:
①FeTiO3中钛元素的化合价为_____;
②氯化中化学方程式为2FeTiO3+6C+7Cl2![]() 2C+2TiCl4+6CO2,则X为_____(填化学式).
2C+2TiCl4+6CO2,则X为_____(填化学式).
③合成中CO和H2以化学计量数1:2恰好完全反应,则该反应的基本反应类型是_____.
④冶炼中氩气的作用是_____,该步反应的化学方程式为_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是初中化学中常见物质间的转化关系,其中,在通常情况下,F、G是组成元素相同的两种气体,若E是生活中常用的调味剂、防腐剂,(部分反应条件略去),试回答下列问题:
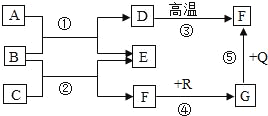
(1)写出物质的化学式为:C_____、D_____、G_____.
(2)反应①的化学方程式为:_____.
(3)图中标出的九种物质按单质、氧化物、酸、碱、盐进行分类,一定没有的物质类别是_____.
(4)反应①~⑤中没有涉及的基本反应类型是_____.
查看答案和解析>>
科目: 来源: 题型:
【题目】通过分析、计算回答下列问题:
(1)相同质量的钠、镁、铝、钾中所含原子个数最多的是_____。
(2)N(NO2)3是科学家发现的一种新型火箭燃料,试计算:
①N(NO2)3的相对分子质量是_____。
②N(NO2)3中氮元素和氧元素的最简质量比是_____。
③N(NO2)3中氮元素的质量分数是_____精确到0.1%)。
(3)取一种可燃物3.2克充分燃烧,测得生成二氧化碳4.4克,水3.6克,试求:
①该可燃物中含有的元素各占多少克_____?(写出完整的计算过程)
②该可燃物的分子中各原子的个数比是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】向盛有20g10%氢氧化钠溶液的烧杯中逐滴滴入7.3%的稀盐酸,下列是关于溶液总质量或溶液pH随盐酸质量变化的关系图(Q点表示恰好完全反应)。其中正确的是

A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面材料,回答问题。
人类赖以生存的环境由自然环境和社会环境组成。自然环境由生物圈、岩石圈、大气圈、水圈组成(如图所示),四个圈层经过漫长演化,既相对稳定、动态平衡,又相互作用、不断变化,各圈层之间的物质和能量不停循环,这些循环既跟物质的组成、结构和性质有关,也受人类活动的影响,并通过复杂的物理变化和化学变化实现。

(一)内涵决定身份﹣﹣物质的组成与分类
(l)用化学符号填空:
岩石圈中含量最高的金属元素是_____。大气圈中含量最高的物质是_____。水圈中含量最高的元素是_____。土壤中能促进农作物根系发达的元素是_____。
(2)按要求填表:
物质所属圈层 | 物质名称 | 物质的化学式 | 用符号表示构成物质的微粒 | 物质类别 |
生物圈 | 蔗糖 | _______ | _______ | _______ |
大气圈 | 氩气 | _______ | _______ | _______ |
水圈 | 氢氧化钙 | _______ | _______ | _______ |
岩石圈 | _______ | _______ | Na+、SiO32﹣ | _______ |
(二)甲烷﹣﹣小分子,大作为
在如图的四大圈层中,有下列6种物质:①甲烷;②水;③二氯化碳;④一氧化碳;⑤氢气;⑥氧气。构成这些物质的分子虽然简单,但这些物质有的是人类赖以生存的基本物质,有的是物质循环关键物质,有的是人类社会生产活动必需的物质。请回答:
(1)在这6种物质中,元素种类共有_____种,人类的生命活动不可缺少的物质有_____(填化学式,下同),植物生长必需的物质有_____,元素种类完全相同的物质是_____。
(2)甲烷是最重要的基础有机物之一,不仅可做燃料,还能发生如下反应:
①在隔绝空气和1000℃条件下,甲烷分解产生炭黑和氢气;
②在隔绝空气和1500℃条件下,甲烷分解产生乙炔和氢气;
③在1400℃条件下,适当比例的甲烷和氧气反应生成氢气和一氧化碳;
④在800℃和催化剂条件下,适当比例的甲烷和二氧化碳反应生成氢气和一氧化碳。
试写出上述②~④三个反应的化学方程式:
②_____;
③_____;
④_____;
(3)在反应①~④中,属于置换反应的有_____。
在反应①和②中,反应物相同,而生成物不同,从微观的角度看,是因为反应条件不同导致_____。
③和④两个反应的反应物不同,但生成物相同,从物质组成的角度看,其原因是_____。
在实际生产中,反应③需要按比例控制氧气不能超量,从物质性质的角度看,原因是_____。
(三)柔之力﹣﹣神奇的水溶液
水在生活、生产和科学实验中应用广泛。岩石圈约有四分之三被水覆盖,其中的某些物质被水溶解,其随水的天然循环在水圈中富集,富集后的物质可能再次沉积到岩石圈。
如图是氯化钠和碳酸钠的溶解度曲线。据图回答下列问题:
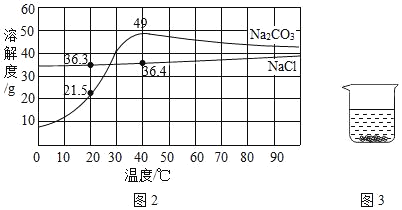
(1)青海湖区的人们有一种经验,冬天捞“碱”、夏天晒盐,这里的“碱”指纯碱,盐指氯化钠,他们所依据的原理是____。
(2)纯碱是一种重要的化工原料,但仅用物理方法从盐湖中“捞碱”远远不能满足需求,工业上主要利用从水圈中获得的食盐来制备纯碱,其反应的化学方程式是_____、_____。
(3)为确定某白色固体是碳酸钠还是氯化钠,在20℃时,取2.5g样品加入盛有10g水的烧杯中,充分搅拌后现象如图所示,则固体粉末是_____。若将该溶液升温到40℃时,则所得溶液溶质质量分数为_____。
(四)金属﹣﹣工业的脊梁
金属及合金广泛应用于生活、生产和航天军工。
资料:水圈和岩石圈中含有丰富的镁元素。工业生产中,可用菱镁矿做原科制'备金属镁,流程如图所示:
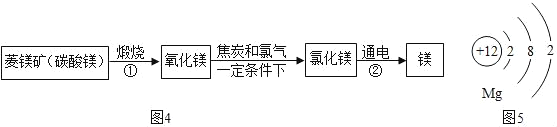
请回答下列问题:
(l)已知①和②属于分解反应,化学方程式分别为_____和_____。
(2)通过化学反应,以岩石圈的矿石为原料还可以制备很多其他金属,请举一例说明(用化学方程式表示其制备原理)_____。
(3)如图是镁原子结构示意图,镁化学性质活泼,原因是_____。四大圈层中含有下列物质:①硫酸锌;②氯化钠;③硫酸;④氢氧化钙;⑤氧气。其中能和铁反应的物质有(填序号)_____。
(4)小梅同学将点燃的镁条伸入盛二氧化碳的集气瓶中,看到镁条剧烈燃烧,发出耀眼白光,瓶壁上有黑色物质生成,她认为这种黑色物质是碳单质。在上述过程中,小梅运用的科学方法有_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】同学们从山上采集到一种石灰石样品,为了测定石灰石样品中碳酸钙的质量分数(石灰石中的杂质不与盐酸反应,也不溶于水),取45g石灰石样品,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示,请计算:

(1)45g这种石灰石样品中碳酸钙的质量是_____g
(2)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
(3)列式计算45g石灰石与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数?_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com