
科目: 来源: 题型:
【题目】结合下列化学实验装置,回答有关问题。
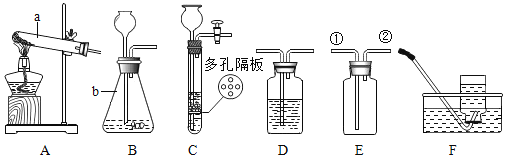
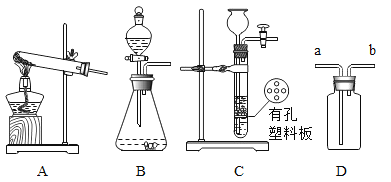
(1)写出图中标有字母的仪器的名称:a___________,b___________ 。
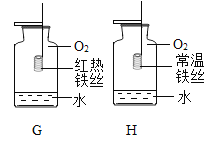
(2)实验室用氯酸钾制取氧气应选择的发生装置是 _______(填代号),反应的化学方程式是__________________,可用_____________法收集氧气。制得的氧气用来做如图所示的实验,发现H中铁丝不燃烧,其原因是__________________。写出G中反应的化学方程式_________________。
(3)实验室制取二氧化碳常用的药品是________________,若用装置E收集二氧化碳,则________________气体应从________(填“①”或“②")端进入;若要获得干燥的二氧化,可将装置B和装置D用胶皮管连接,并在装置D中盛放________________(填物质名称)试剂。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题。

①P点的含义_________________________________
② t3℃ 时,将30g甲物质加入到50g水中,充分溶解
后所得溶液的质量为_________________________________
③当甲中含少量乙时,提纯甲的方法是______________________
④ t3℃ 时等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液中溶剂的质量由大到小的顺序为
查看答案和解析>>
科目: 来源: 题型:
【题目】下图为干电池的结构示意图,请利用所学知识完成下列问题。

(1)碳棒(主要成分是石墨)用作干电池的正极是利用了石墨的______性。
(2)干电池的材料很多可以回收利用,例如双氧水与回收的二氧化锰可用于实验室制取氧气。写出该反应的化学方程式: ;
(3)黄铜是铜与锌的合金,其硬度 (填“大于”或“小于”)纯铜。将足量的锌片放入硫酸铜溶液中,观察到 的现象,说明锌比铜活泼。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学用语是学习化学的重要工具,是国际通用的化学语言。请用化学用语填空:
①氯化亚铁中铁元素的化合价_______;
②两个氢原子_______;
③三个二氧化硫分子______;
④四个氢氧根离子_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】“中国制造”“一带一路”等基础建设都需要用到大量钢铁。
(1)认识铁及其应用
①从微观角度看,铁是由____(填化学符号)构成,其在地壳中的含量居所有元素第____位。
②生铁和钢均是生活中常见的金属材料,它们都属于 __(填“纯净物”或“混合物”)。
③铁锅可用以烹饪,利用了铁的_____性。很多人认为:铁锅炒菜过程中会有少量铁进入人体,与胃液中的盐酸反应,请写出铁与稀盐酸反应的化学方程式_____,该反应的基本反应类型为_____,所以用铁锅炒菜能“补铁”,这里的“铁”指______(填“原子”“单质”或“元素”)。
(2)铁的冶炼
某化学实验小组利用下图装置模拟铁的冶炼并测定某赤铁矿石中氧化铁的质量分数(假设赤铁矿中杂质不参与反应)。
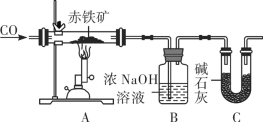
①实验开始时,先进行的操作是____(填字母)。
a 通入一氧化碳 b 加热
②实验过程中观察到装置A中玻璃管内发生的现象是______。
③写出B装置发生反应的化学方程式是__________。
④从环境保护的角度看此实验存在的缺陷是__________。
⑤实验前称量赤铁矿石的质量为20g,通入足量一氧化碳充分反应,测得B装置总质量增加13.2 g。若不考虑实验过程中水分带出的影响,则装置C的作用是________;求该赤铁矿石中氧化铁的质量分数______(请写出计算过程)。
(3)铁的防护
①铁制品暴露于潮湿的空气中,易形成铁锈。由于铁锈结构特点是______,故铁制品表面的铁锈应及时清除,用稀盐酸适时浸泡是清除铁锈的方法之一,铁锈的主要成分与盐酸反应的化学方程式为_________。
②家庭使用的铁锅防锈方法有___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】碳酸钠、碳酸氢钠是生活中两种常见的重要的盐。
(1)碳酸钠(俗称纯碱、苏打)与碳酸氢钠(俗称_____),均为________色固体,水溶液均呈_______性,向它们的水溶液中分别滴入无色酚酞试液,酚酞试液均变红色。
(2)碳酸钠、碳酸氢钠均可与稀盐酸反应,其中碳酸钠与稀盐酸反应的化学方程式为_____。但是,碳酸钠、碳酸氢钠与稀盐酸反应产生二氧化碳的速率是否相同?校兴趣小组同学针对于此,展开探究:
(方案设计)
①甲设计的实验如图1所示,实验时,同时全部推出足量稀盐酸后,观察到图2所示现象。于是他得出______和稀盐酸反应产生二氧化碳较快的结论。
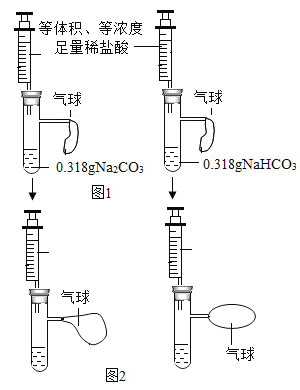
②乙同学通过计算可知:0.318 g碳酸氢钠约产生0.167 g二氧化碳,而0.318 g碳酸钠产生二氧化碳的质量为______g,等质量的碳酸钠与碳酸氢钠与足量的稀盐酸作用,碳酸氢钠产生二氧化碳的质量更多,显然甲同学的设计不妥,应取含碳元素质量相同的碳酸钠和碳酸氢钠进行实验。若碳酸钠的质量仍为0.318g,应称取碳酸氢钠的质量为_______g。
③小组同学在老师指导下设计了图3所示实验。连通管除消除稀盐酸滴入占有体积引起的误差,还有______的作用。
分别取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠稀溶液(各滴2滴酚酞溶液)以及相同体积、相同浓度的足量稀盐酸进行实验。实验时,广口瓶内压强随时间变化如图4所示,溶液颜色变化记录如表1。
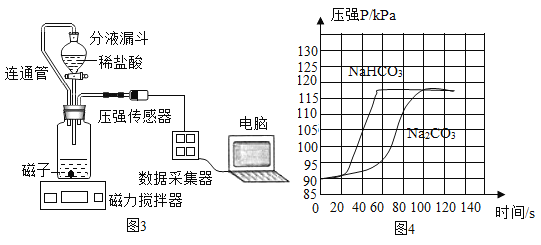
表1:
滴入酚酞溶液 | 滴入稀盐酸,溶液颜色变化 | |
碳酸钠溶液 | 红色 | 红色→浅红色→无色 |
碳酸氢钠溶液 | 浅红色 | 淺红色→无色 |
(实验结论)分析图4所示的实验数据可得到:相同条件下,碳酸氢钠与稀盐酸反应产生二氧化碳速率更快,你判断的理由是_______。
(实验反思)小组同学分析表1实验现象和图4数据,得出碳酸钠能与稀盐酸反应产生二氧化碳,反应是分步进行的。第一步发生的化学反应方程式是:_______,第二步发生的反应是:NaHCO3+HCl=NaCl+H2O+CO2↑。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国煤炭资源丰富。目前人们除了将煤作为燃料外,更关注煤化工技术。工业上以煤和空气为原料生产尿素[CO(NH2)2]的一种流程如下:
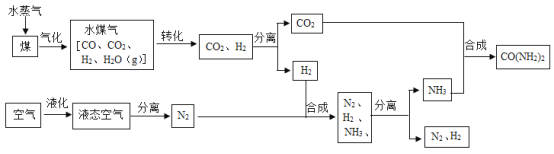
(1)从液态空气中分离出N2的过程属于_____(填“物理”或“化学”)变化。
(2)在煤和水蒸气反应前需先将煤粉碎,这样做的目的是______。
(3)水煤气在铜催化下实现CO的转化:CO+H2O![]() CO2+X,其中X的化学式为____。
CO2+X,其中X的化学式为____。
(4)上述流程中,在一定条件下合成尿素的同时还有水生成,该反应的化学方程式为____。
(5)实际生产中,反应不可能完全进行。上述流程中可以循环利用的物质有______。
(6)合成的尿素[CO(NH2)2]是重要的化学肥料,区分尿素与硫酸铵[ (NH4)2 SO4]可进行以下操作:分别取样于试管中,加入氢氧化钠溶液并加热,在试管口放一张湿润的______色石蕊试纸,观察颜色变化。
查看答案和解析>>
科目: 来源: 题型:
【题目】水是宝贵的自然资源。
(1)河水经处理后可用作城市生活用水,自来水厂净水的过程中不包括的净水方法是____。
a 沉降 b 吸附 c 蒸馏 d 消毒
(2)河水中若含有难溶性杂质,可以通过过滤的方法除去。用下图装置对河水水样进行过滤,下列关于过滤的说法中正确的有____(填字母)。
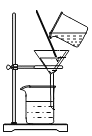
a 用玻璃棒引流
b 滤纸边缘高出漏斗
c 漏斗下端尖嘴未紧靠烧杯内壁
d 将滤纸湿润,使其紧贴漏斗内壁
e 用玻璃棒在漏斗中轻轻搅动以加快过滤速度
f 利用过滤操作,可以将氯化钠从氯化钠溶液中分离出来
(3)若要检验过滤后的液体是否为硬水,可以加入_____,搅拌后,观察现象。
(4)保护水资源是我们义不容辞的责任。下列做法不合理的有_____(填字母)。
a 严格监管化肥和农药的使用 b 不间断地放水洗衣服
c 积极探索污水处理的新技术 d 抑制水中所有动、植物的生长
(5)在盛有水的烧杯中加入一定量硝酸铵,形成溶液过程中,温度会_____(选填“升高”“降低”或“不变”)。
(6)水中加入洗涤剂能洗掉餐具上的油污,这是利用了洗涤剂的_____作用。
查看答案和解析>>
科目: 来源: 题型:
【题目】二维价类图可有效帮助我们建立物质之间的联系,高效进行化学学习。

(1)常见的碳单质有金刚石、石墨等,其中常用作电池电极的是_____(填“金刚石”或“石墨”)。
(2)钙____(填“是”或“不是”)人体所需的微量元素,儿童缺钙易得_____(填字母)。
A 侏儒症 b 佝偻病 c 贫血病 d 白内障
(3)碳酸钙由Ca2+和____(填符号)构成,碳酸钙中钙元素的质量分数为_____。
(4)请写出CO燃烧生成物质M的化学方程式_____,从热效应的角度分析,该反应____热量(填“吸收”或“释放”),可见:含碳物质的不完全燃烧,不但会产生污染,而且存在____的问题。
(5)实验室制备M气体,可控制反应发生与停止的发生装置是____(填符号)。若用D装置收集M气体,则气体从 __端通入(填“a”或“b”),验满的操作是 _____;若用该装置检验M气体,则气体从____端通入(填“a”或“b”),如果含有M气体,则发生反应的化学方程式为____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com