
科目: 来源: 题型:
【题目】“对比法”是实验探究中常用的一种科学方法。分析以下铁钉生锈实验的设计、得出的结论不正确的是( )
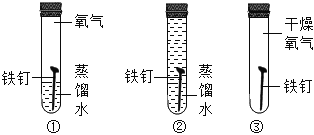
A.对比①②可以说明铁生锈一定要有氧气参加
B.对比②③可以说明铁生锈一定要有水参加
C.对比①③可以说明铁生锈一定要有水参加
D.对比①②③可以说明铁生锈必须水和氧气同时参加
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物R和氧气置于完全封闭的容器中引燃,充分反应后,生成二氧化碳和水。实验测得反应前后物质质量如下表:
R | O2 | CO2 | H2O | |
反应前质量(g) | 51 | 96 | 0 | 0 |
反应后质量(g) | x | 0 | 88 | 54 |
下列说法中不正确的是()
A.x的值为5
B.R物质中只含有碳、氢元素
C.R物质中碳氢元素的质量比为4∶1
D.反应生成的二氧化碳和水的分子个数比为2∶3
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。
(1)请写出镁条与氧气反应的化学方程式_______________。
(2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律。我_____(“同意”或“不同意”)小明的观点,因为__________________。
(3)小红按如图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。
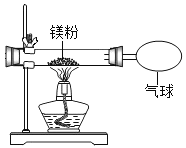
(提出问题)黄色固体是什么呢?
(查阅资料)①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。
(做出猜想)黄色固体是Mg3N2
(实验探究)请设计实验,验证猜想
实验操作 | 实验现象 | 结论 |
取少量黄色固体于试管中,加入适量的水,并将____________ | ___________________ | 证明猜想正确 |
(反思与交流)空气中N2的含量远大于O2的含量,而镁条在空气中燃烧生成的MgO却远多于Mg3N2。请给出合理的解释______________________,写出生成Mg3N2的化学方程式____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(4分)乙炔(![]() )是生产聚氯乙烯的重要原料。用电石(主要成分为
)是生产聚氯乙烯的重要原料。用电石(主要成分为![]() )与水反应可制取乙炔,最终还可得到电石渣。某电石渣中含氢氧化钙
)与水反应可制取乙炔,最终还可得到电石渣。某电石渣中含氢氧化钙![]() ,其余为杂质,此电石渣可用于处理电镀厂排出的酸性废水。
,其余为杂质,此电石渣可用于处理电镀厂排出的酸性废水。
(1)乙炔中碳、氢元素的质量比为 。
(2)100kg上述电石渣中氢氧化钙的质量为 ![]() 。
。
(3)用上述电石渣处理含硫酸![]() 的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),求至少需要电石渣的质量(写出计算过程及结果)。
的酸性废水(假设电石渣中的杂质、废水中其他成分均不参加反应),求至少需要电石渣的质量(写出计算过程及结果)。
查看答案和解析>>
科目: 来源: 题型:
【题目】化学是一门以实验为基础的学科,根据下图回答问题:

(1)写出仪器名称:a______, b______。
(2)实验室用氯酸钾和二氧化锰制取氧气,选用的发生装置是______(填字母序号),其中二氧化锰的作用为______。
(3)硫化氢为无色气体,密度比空气的密度大,有臭鸡蛋气味,有剧毒,能溶于水,其水溶液为氢硫酸,可用硫化亚铁(FeS)固体与稀硫酸反应制得。制取硫化氢气体选用的发生装置是____,收集装置是____,反应的化学方程式__________________,操作必须在通风橱中进行,原因是_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(7分)现代循环经济要求综合考虑环境污染和经济效益。高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:[(NH4)2CO3溶液呈碱性,40 ℃以上时(NH4)2CO3分解]。
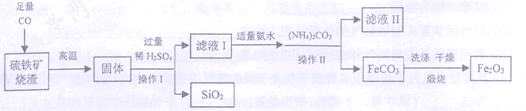
(1)实验室中,操作Ⅰ、操作Ⅱ用到的玻璃仪器有玻璃棒、烧杯、 等。
(2)滤液Ⅰ中主要的阳离子是 等。
(3)加适量氨水的目的是 。
(4)根据题中信息,加入(NH4)2CO3后,该反应必须控制的条件是 。
(5)滤液Ⅱ中可回收的产品是 (写化学式)。
(6)写出在空气中煅烧FeCO3的化学反应方程式 。
查看答案和解析>>
科目: 来源: 题型:
【题目】盐酸是一种重要的化工产品,也是实验室中重要的化学试剂,用途广泛。
(1)增大压强,HCl由气态变为液态,从微观的角度分析该变化过程中改变的是_____________。
(2)蘸浓盐酸的玻璃棒和蘸浓氨水的玻璃棒接近但不接触,发生了如图的现象,反应的化学方程式是______________,浓盐酸和浓氨水都具有挥发性,气体有刺激性气味和腐蚀性,实验时要注意____________。
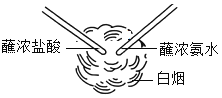
(3)观察如图并回答问题:
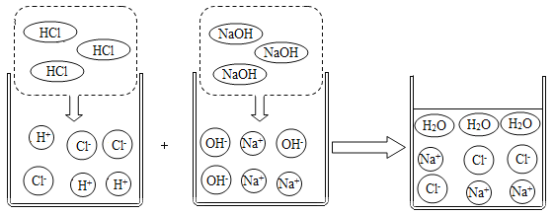
由如图可知,HCl与NaOH的反应实质是H+ 和OH- 之间的反应,此反应可表示为:H++OH-=H2O。像这种用实际参与反应的离子来表示反应的式子称为离子方程式。任何复分解反应都可用离子方程式来表示。
[练习] 按照书写化学方程式的要求写出下列反应的离子方程式
HCl溶液与AgNO3 溶液反应_____________________。
HCl溶液与Na2CO3溶液反应_____________________。
[归纳] 复分解反应的实质是:阴阳离子结合生成___________________的反应。
[应用] 判断在水溶液中一定能大量共存的离子组是___________ 。
A Na+、H+、Cl-、CO32- B H+、Ba2+、Cl-、SO42-
C Cu2+、Na+、NO3-、OH- D H+、K+、Cl-、SO42-
查看答案和解析>>
科目: 来源: 题型:
【题目】下图表示的是KNO3和NaNO3的溶解度曲线。下列说法正确的是
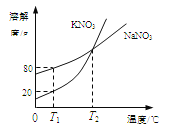
A.T2℃时,KNO3溶液的浓度一定等于NaNO3溶液的浓度
B.T1℃时,在50g水里加入15g KNO3固体,充分溶解,可得到65g溶液
C.T1℃时,往180g NaNO3饱和溶液中加入620g水可配成质量分数为10%的NaNO3溶液
D.若KNO3中混有少量NaNO3,可用蒸发溶剂的方法提纯
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图像分别对应四个变化过程,其中正确的是
A.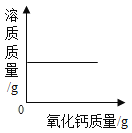 一定量的饱和石灰水中加入氧化钙
一定量的饱和石灰水中加入氧化钙
B. 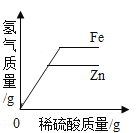 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应
C.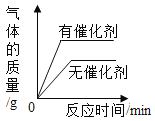 等体积,等浓度的双氧水制取氧气
等体积,等浓度的双氧水制取氧气
D.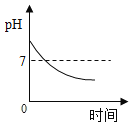 服用胃舒平[主要成分Al(OH)3]治疗胃酸过多,胃液pH的变化
服用胃舒平[主要成分Al(OH)3]治疗胃酸过多,胃液pH的变化
查看答案和解析>>
科目: 来源: 题型:
【题目】如图的反应中,甲、乙、丙三种分子的个数比为1︰3︰2,则从图示中获得的信息正确的是
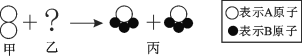
A.生成物一定属于氧化物 B.原子种类在化学反应中发生了变化
C.该反应不可能是分解反应 D.乙分子中A与B的原子个数比为1∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com