
科目: 来源: 题型:
【题目】某化学兴趣小组做粗盐(含有难溶性杂质)提纯实验,并用所得的精盐配制50g 5%的氯化钠溶液。
实验一:如图是同学做粗盐提纯实验的操作示意图,回答下列问题:
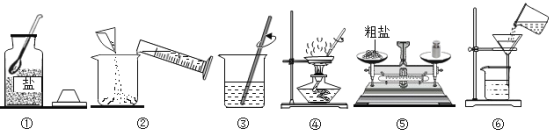
(1)操作③中用玻璃棒搅拌的作用是_________。
(2)操作⑥中的错误是________。
(3)操作④中,当观察到_________时,停止加热。
实验二:用提纯得到的精盐配制50g 5%的氯化钠溶液,经检测,所配溶液溶质质量分数偏小,其原因可能有_________(填序号)。
①氯化钠固体仍然不纯 ②量取水时,仰视读数 ③配好装瓶时,有少量溶液洒出
查看答案和解析>>
科目: 来源: 题型:
【题目】人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色。
(1)人们习惯上把金、银、铜、铁、锡五种金属统称为“五金”,在“五金”顺序中把金属____的位置移到最后,正好符合由弱到强的顺序。
(2)汽车车体多用钢材制造。表面喷漆不仅美观,而且可有效防止______。
(3)工业冶炼金属:
①工业上用CO还原赤铁矿冶炼金属铁的化学方程式为________。工业冶铁是复杂的过程,把铁矿石、石灰石和_______、一起加入高炉;石灰石首先在高温下发生分解,其化学反应方程式为_______;其分解产物与铁矿石的杂质结合成炉渣。
②中国古老的冶铜方法“湿法冶铜”主要的反应原理是_________(写化学方程式)。
(4)在实验室中探究铝、铜、银的金属活动性顺序,除铝、银外,还需要用到的试剂是___(填化学式)。
(5)铁锅、铝锅是生活中常用的炊具,如图是铁锅的示意图。

①使用铁锅是利用金属的_______,
②家庭用的燃料大多为天然气,写出天然气燃烧的化学方程式_______。
查看答案和解析>>
科目: 来源: 题型:
【题目】生活中处处蕴含着化学知识。请用所学知识回答下列问题:
(1)高安建山镇的富硒农产品(红薯粉皮,大米,黑芝麻,紫薯等)深受老百姓的喜爱,这里的富“硒”指的是_____。(填“原子”“分子”“单质”或“元素”)
(2)2018年11月12日起中国流动科技馆高安站巡展启动,在展区看到了金刚石的微观结构模型,构成金刚石的基本粒子是_____。
(3)高安是中国书法之乡。用墨(含碳)写的字可以长时间保存,所利用的碳的化学性质是_____。
(4)高安陶瓷产业享誉全国。工业上制造高温结构陶瓷碳化硅(SiC)主要是以SiO2和C为原料,在高温条件下生成碳化硅和一种有毒气体,则其化学方程式为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】2019年10月9日,97岁高龄的约翰·B·古迪纳夫获得诺贝尔化学奖,他在锂离子电池研究方面做出了突出贡献,被业界称为“锂电池之父”。
(1)石墨可以用来做干电池的电极,是因为石墨_____。
(2)LiMn2O4是锂离子电池的一种正极材料,制备LiMn2O4的化学反应方程式为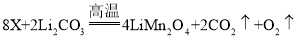 ,该反应中物质X的化学式为_____,LiMn2O4中锂元素与氧元素的质量比为_____。
,该反应中物质X的化学式为_____,LiMn2O4中锂元素与氧元素的质量比为_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是 a、b、c 三种物质的溶解度曲线。
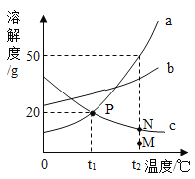
(1)点P表示__________;
(2)要使M点的c溶液变成N点的c溶液,可采取的一种措施是_____________;
(3)当a中含有少量的 b,要得到纯净的 a,可采用的方法是____________________;
(4)t2℃时,等质量的a、b、c三种物质的饱和溶液降温到t1℃时,三种溶液的质量分数由大到小的顺序______________;
(5)t2℃时,40ga物质加入到40g水中形成______g溶液。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图像能正确反映其对应实验操作的是
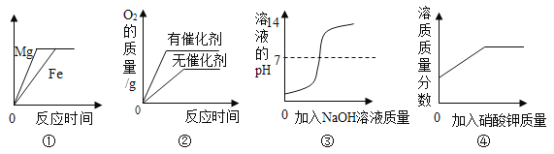
A.①等质量的镁、铁分别加入到足量的同浓度的稀盐酸中
B.②用等质量、等浓度的双氧水分别制取氧气
C.③向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
D.④某温度下,向一定量饱和硝酸钾溶液中加入硝酸钾晶体
查看答案和解析>>
科目: 来源: 题型:
【题目】化学课外活动小组的某位同学在实验室用氯酸钾和二氧化锰的混合物制取氧气,并对反应后固体剩余物进行回收、利用,实验操作流程及数据记录如下:

请回答下列问题:
(1)该同学制得氧气的质量为________g。
(2)计算滤液中溶质质量分数。(忽略水的损耗,写出计算过程)
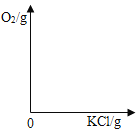
(3)在图中画出氯酸钾分解生成KCl和O2的质量关系图。并在坐标轴上标出一组对应数据。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组用如图所示装置进行如下实验(不考虑气体与水或盐的反应)。
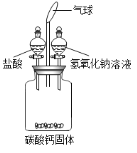
(1)先向广口瓶中加入一定量盐酸溶液,关闭活塞,震荡,观察到固体全部溶解,气球变大。然后再将一定量氢氧化钠溶液加入广口瓶中,关闭活塞,震荡,发现气球明显变小,同时在广口瓶中还能观察到的现象是___________________, 用化学方程式表示该现象产生的原因:_____________________________________。
(2)实验结束后,同学们对广口瓶中的溶液进行探究。
(提出问题)广口瓶中的溶液含有哪些溶质?
(交流讨论)小明取广口瓶中溶液少量加入试管内,向其广口瓶中加入过量稀盐酸,发现有气泡产生,由此他得出结论:广口瓶中溶液的溶质组成为Na2CO3、NaCl、CaCl2。大家一致认为小明的结论是不正确的,理由是________________________________。后经大家讨论,达成共识,对广口瓶溶液中溶质组成的判断只有两种结论,结论一:组成为__________________________两种溶质,结论二:组成为____________________________________ 三种溶质。
(3)(实验设计)
实验步骤 | 实验现象 | 实验结论 |
①取广口瓶中溶液少量于试管中,向其中加入过量的________溶液 | 有白色沉淀产生 | 结论一是正确的 |
②向步骤①所得的溶液中加______________ | ______________ |
反思讨论:第①步加入试剂要求过量的作用是:________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】钛和钛合金被认为是 21 世纪的重要金属材料,他们具有很多优良的性能,如熔点高,密度小,可塑性好,耐腐蚀,常温下不易与酸和碱发生反应等。以某钛铁矿(主要成分为FeTiO3,同时含有少量的Fe3O4等)为原料制TiO2,再由TiO2制金属 Ti 的工艺流程如下:
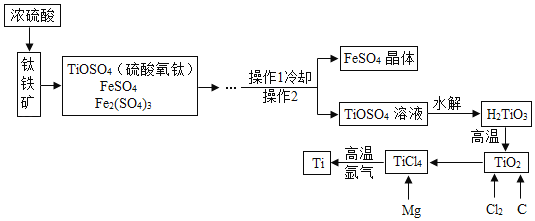
(查阅资料)
一、钛、镁在高温下与空气中的氧气、二氧化碳等反应。
二、Fe3O4中的铁元素化合价既有+3价,也有+2价,可以把Fe3O4 看作“Fe2O3 FeO”。
(1)浓硫酸具有强烈的_______________________,所以使用时要注意安全,避免溅到皮肤或衣物上。
(2)操作 2 的名称是_________。
(3) TiO2可与焦炭、氯气按照一定的质量比在高温下反应,生成TiCl4和一种可燃性气体,该气体为_____。(填写化学式)。小聪要称取8.5g焦炭粉,手头的天平只配有一个规格为10g的砝码,该天平游码标尺的最大值5g,要一次性称出8.5g焦炭粉,则游码须移到刻度为_____g处;面向天平,砝码放于____盘。(填“左”或“右”)
(4)工业上常在高温和氩气氛围中,用金属镁和TiCl4反应的方法制备 Ti,同时生成一种化合物,该反应的基本类型为:_____________,氩气的作用是_______________。所得金属钛中含有少量的金属镁,若要除去金属钛中的少量镁,并确保充分反应后溶液中只含同一种盐,则可加入的试剂是________(填试剂名称)。
(5)试写出Fe3O4与稀硫酸反应的化学方程式:_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是实验室常用的部分实验装置,请按要求回答问题。
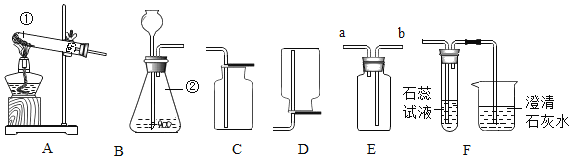
(1)写出标有编号的仪器名称:①_____,②_____。
(2)用加热高锰酸钾的方法制取氧气,所选择的发生和收集装置是_____(填字母序号),写出反应的化学方程式_____;检验氧气收集满的方法是_____。
(3)将装置B、E、F相连接用于制取二氧化碳气体并验证其化学性质,若E装置中装有饱和碳酸氢钠溶液,则F装置中可观察到的现象:试管中石蕊溶液_____,烧杯中澄清石灰水_____。
(4)下列实验的相关说法不正确的是_____(填数字序号)。
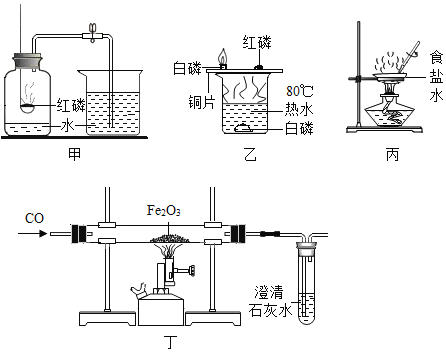
①甲实验中,红磷要过量
②乙实验中,水中的白磷没有燃烧,是因为白磷没有跟氧气充分接触
③丙实验中,搅拌的目的是防止局部温度过高,造成液滴飞溅
④丁实验开始时,先加热,后通入一氧化碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com