
科目: 来源: 题型:
【题目】水和溶液与我们的生活息息相关。
(1)将厨房中的下列物质放入水中,能形成溶液的是____________________。
A 牛奶 B 香油 C 面粉 D 白糖
(2)生活中常用_______________方法降低水的硬度,并起到杀菌消毒的作用。
(3)妈妈衣服上沾了油污,小明建议妈妈不要直接用水清洗,而是先用酒精或洗洁精清洗,请分别解释它们去油的原理_________________。
(4)甲、乙、丙三种固体物质的溶解度曲线如下图所示,回答下列问题:
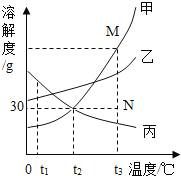
① 在 t2℃时,把 30g 甲溶解于 50g水中得到溶液的质量为_________________
② 将图中 N 点的甲溶液转化为M的甲溶液的方法是_________________
③ 将甲、乙、丙三种物质的饱和溶液从 t3℃降到 t2℃,溶质的质量分数的大小关系是_________。
④ 要配制等质量的 t3℃的甲、乙、丙三种物质的饱和溶液, 所需水的质量关系是__________。配制过程中若量取水时俯视读数,则会造成所配溶液的质量分数___________。(“偏大”或“偏小”)
查看答案和解析>>
科目: 来源: 题型:
【题目】铁是目前世界上使用最多的金属。
(1)认识铁:从宏观看,铁由__组成;从微观看,铁由________ 构成。
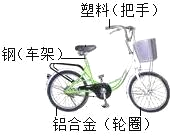
(2)生活中:“共享单车”作为代步工具,既轻便灵活,又环保。如图是一款自行车的图片,所标材料中属于金属材料的有_________,铝合金轮圈不易生锈的原因是__________。
(3)工业上:用铁矿石炼铁,其设备是__________,原料是_____________。
(4)实验室:用下图模拟炼铁。实验的主要过程如下:取少量 Fe2O3 装入“V”型管中, 用针筒抽取足量 CO 至最大刻度,小针筒内抽取 2mL 澄清石灰水,打开止水夹,推动左 侧注射器移动至 1/3 刻度处,后关闭止水夹;在点燃酒精灯的同时轻轻推动左侧注射器。 反应一段时间后,右侧注射器中澄清石灰水变浑浊,停止加热。
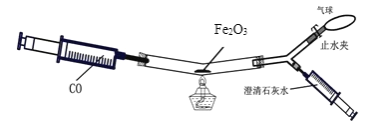
①点燃酒精灯前先推动左侧注射器的原因是_____________。
②写出“V”型管中的化学反应方程式______________。
③检验反应后所得固体中是否有铁的方法是____________________。(写出具体的操作步骤和现象)
查看答案和解析>>
科目: 来源: 题型:
【题目】向 100g 水中不断加入固体 A 或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )
![]()
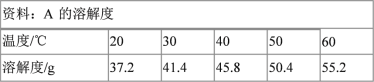
A.②中 A 的质量分数最大B.③⑤中 A 的质量分数相等
C.②④⑤的溶液为饱和溶液D.①③④⑤中没有固体存在
查看答案和解析>>
科目: 来源: 题型:
【题目】下列图象与所述操作过程相符的是( )
A.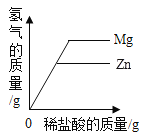 向同质量的镁条和锌片滴加同浓度的稀盐酸
向同质量的镁条和锌片滴加同浓度的稀盐酸
B.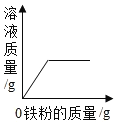 向一定量硫酸铜溶液中不断加入铁粉
向一定量硫酸铜溶液中不断加入铁粉
C. 将 60℃接近饱和的硝酸钾溶液恒温蒸发水 分
将 60℃接近饱和的硝酸钾溶液恒温蒸发水 分
D.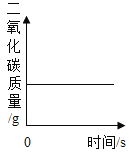 木炭在盛有O2 密闭容器内燃烧
木炭在盛有O2 密闭容器内燃烧
查看答案和解析>>
科目: 来源: 题型:
【题目】在点燃条件下,A 和 B 反应生成 C 和 D,反应前后分子种类变化的微观示意图如图所 示。下列说法不正确的是( )
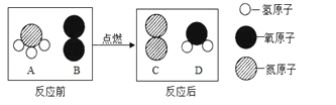
A.A 物质是由 3 个氢原子和 1 个氮原子构成的
B.在该反应中,生成 C 和 D 的质量比为 14:27
C.该反应是置换反应
D.该反应前后分子的总数发生了改变
查看答案和解析>>
科目: 来源: 题型:
【题目】已知氧化铜样品中主要成分是CuO,还含有少量杂质。为了测定样品中氧化铜的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析。
(资料1)草酸晶体(H2C2O4·3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4·3H2O ![]() CO2↑+ CO↑+ 4H2O
CO2↑+ CO↑+ 4H2O
(资料2)浓硫酸具有吸水性,是常见的液态干燥剂。碱石灰是生石灰和氢氧化钠的固体混合物,是常见的干燥剂,能吸收水和二氧化碳。
(1)下列可用作草酸分解制取气体的装置是__________(填字母编号)。
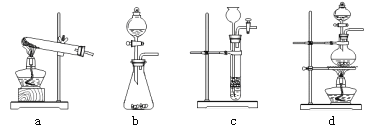
(问题讨论)用下图所示装置进行实验:
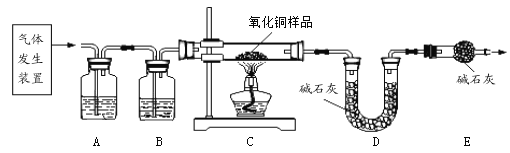
(2)实验前应先_____________。
(3)进入C中的气体是纯净、干燥的CO,则A、B中的试剂依次是___________(填字母编号)。
a 浓硫酸 b 足量的澄清的石灰水
(4)A装置的作用是__________,写出相应的方程式_____________。
(5)对C装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前_______________。 ②停止加热后________________。
(数据分析与计算)
称取氧化铜样品10.0g,用上述装置进行实验,完全反应后,称得C装置中剩余固体的质量为8.4g,求原样品中氧化铜的质量分数______________?(写出计算过程)
(实验评价)
反思1:请指出(问题讨论)中实验装置的一个明显缺陷__________。
反思2: 本实验中如果缺少B装置(不考虑其它因素),则测得样品中氧化铜的质量分数与实际值相比会__________(填“偏小”、“不变”或“偏大”)。
反思3:不用上述方法,通过测定________ 装置(填序号)的质量变化,也可以获得氧化铜质量的分数。
查看答案和解析>>
科目: 来源: 题型:
【题目】能源的煤气化和液化流程示意图如下图所示,请结合图像回答问题:
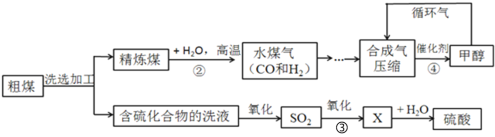
(1)精炼煤中主要成分是碳,步骤②中发生反应的化学方程式为_________________。
(2)步骤③中,SO2进一步氧化得到X,X为硫的另一种氧化物,其中硫元素的化合价为+6价,X的化学式为________。
(3)经过进一步净化,含较多杂质的水煤气转化为合成气(CO和H2的混合气体),步骤④中生成的甲醇(CH3OH)是一种重要的化工原料,该反应的化学方程式为______________
(4)循环气的主要成分是__________和少量未完全分离出去的甲醇。
(5)从“绿色化学”的角度分析,“煤的气化和液化”流程的优点:__________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图是实验室常用的实验装置,请回答下列问题。

(1)写出仪器①的名称_________ 。
(2)用高锰酸钾制取氧气,选用的发生装置是________(填序号),反应的化学方程式为______,为防止高锰酸钾粉末进入导管,该装置需做一点改进的是_____,若用D装置收集氧气,当观察到气泡_____冒出时,便可开始收集。
(3)实验室制取二氧化碳应选用的一组装置是_______(填序号),反应的化学方程式是_______。图E是某同学利用报废试管设计的制二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点:_______。
(4)用收集的氧气完成图F铁丝燃烧的实验,反应的化学方程式为___________。
(5)某化学兴趣小组在老师指导下制取、干燥、收集氨气,并探究氨气的一些性质.
(查阅资料)
a.氨气通常情况下是有刺激性气味的无色气体,密度比空气小,极易溶于水.
b.氨水是氨气(NH3)的水溶液,具有碱的性质。
c.碱能使无色酚酞溶液变红。

图为合成氨的模拟实验装置图(玻璃管中是铁粉和石棉绒组成的混合物)。步骤:①检查气密性;②使锌粒和稀硫酸反应一段时间;③在Y型管盛有亚硝酸钠和氯化铵饱和溶液的一边加热(NH4Cl + NaNO2 ![]() NaCl + 2H2O + N2↑ );④到产生氮气较快时,再点燃玻璃管下方的酒精灯进行加热。
NaCl + 2H2O + N2↑ );④到产生氮气较快时,再点燃玻璃管下方的酒精灯进行加热。
①反应开始前使锌粒和稀硫酸反应一段时间的目的是:_______。
②当锥形瓶中出现________ 现象,表示有氨气生成。
③写出玻璃管中生成氨气的化学方程式_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)现有H、C、O、S Ca四种常见的元素,请选用其中的元素写出符合下列要求的物质各一种(用化学式表示):
①人体内含量最多的物质 __________; ②常用来做铅笔芯的物质是_____;
③可造成酸雨的气体______________; ④酒精灯内的燃料____________。
(2)下图是包含物质A、B、C、D和单质碳卡片的“化学拼图”,相邻两张卡片所标的物质间能发生反应, 其中A、B、C均为气体,B、C的组成元素相同。D是一种黑色固体。
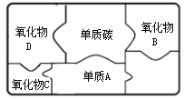
①A是_________,B是________________。
②D物质是铁与单质A反应的产物,写出单质碳与D反应的化学方程式为_________。
③B与单质碳反应的化学方程式为____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】取一定质量的CaCO3高温加热一段时间后,冷却,测得剩余固体的质量为12.0 g,剩余固体中钙元素质量分数为50.0%。下列判断正确的是
A.生成3.0 g CO2气体B.剩余CaCO3的质量为3. 3 g
C.生成了8.4 g CaOD.原来CaCO3的质量为16.3 g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com