
科目: 来源: 题型:阅读理解
 海洋资源十分丰富.
海洋资源十分丰富.
| 实验序号 | 第一次实验 | 第二次实验 | 第三次实验 |
| 所取海水质量/kg | 100 | 100 | 100 |
| 生成沉淀质量/kg | 0.28 | 0.29 | 0.30 |
查看答案和解析>>
科目: 来源: 题型:
 29、用图进行CO和CO2的分离与干燥(其中A为弹簧夹,B为分液漏斗活塞),请填写下列空白:
29、用图进行CO和CO2的分离与干燥(其中A为弹簧夹,B为分液漏斗活塞),请填写下列空白:查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
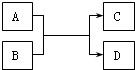 26、A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).
26、A、B、C、D都是初中化学中常见物质,它们间关系如图所示(反应条件已省略).查看答案和解析>>
科目: 来源: 题型:
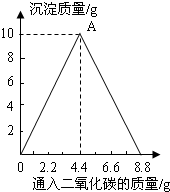 已知CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的澄清石灰水中通入CO2,产生沉淀的质量与通入CO2气体的质量的关系如图所示,回答下列问题:
已知CaCO3+H2O+CO2=Ca(HCO3)2,Ca(HCO3)2易溶于水.某实验小组在含一定量Ca(OH)2的澄清石灰水中通入CO2,产生沉淀的质量与通入CO2气体的质量的关系如图所示,回答下列问题:查看答案和解析>>
科目: 来源: 题型:
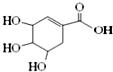 23、“达菲”是世界卫生组织认可的抗甲型H1N1流感病毒的药物,生产达菲的主要原料莽草酸(化学式为C7H10O5,其结构如图,碳原子和部分氢原子未标出)有75%是从八角中提炼的.莽草酸是一种白色粉末,易溶于水,难溶于有机溶剂.熔点185℃~191℃.
23、“达菲”是世界卫生组织认可的抗甲型H1N1流感病毒的药物,生产达菲的主要原料莽草酸(化学式为C7H10O5,其结构如图,碳原子和部分氢原子未标出)有75%是从八角中提炼的.莽草酸是一种白色粉末,易溶于水,难溶于有机溶剂.熔点185℃~191℃.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com